Medicinsk expert av artikeln
Nya publikationer
Hypofysmikroadenom: orsaker, symtom, vad som är farligt, prognos
Senast recenserade: 23.04.2024

Allt iLive-innehåll är mediekontrollerat eller faktiskt kontrollerat för att säkerställa så mycket faktuell noggrannhet som möjligt.
Vi har strikta sourcing riktlinjer och endast länk till välrenommerade media webbplatser, akademiska forskningsinstitut och, när det är möjligt, medicinsk peer granskad studier. Observera att siffrorna inom parentes ([1], [2] etc.) är klickbara länkar till dessa studier.
Om du anser att något av vårt innehåll är felaktigt, omodernt eller på annat sätt tveksamt, välj det och tryck på Ctrl + Enter.
Neoplasmer av godartad natur som uppstår i de endokrina körtlarna kallas adenom, och hypofysmikroadenomen är en liten tumör i dess främre lob, som producerar ett antal viktiga hormoner.
Epidemiologi
Förekomsten av hypofystumörer uppskattas till 10-23 % och hypofysadenom, som kan ha olika former och storlekar, är de vanligaste (16 %). [1]
Upp till 20-25% av människor kan ha små hypofystumörer - mikroadenom, utan att ens veta om det, och sådana tumörer upptäcks i ungefär hälften av fallen av en slump under hjärnavbildning.
Prolaktinutsöndrande mikroadenom står för 45-75 % av dessa tumörer; andelen ACTH-producerande formationer står inte för mer än 14 % av fallen och frekvensen av STH-producerande mikroadenom överstiger inte 2 %.
Hypofysmikroadenom hos barn och ungdomar upptäcks i 10,7-28% av fallen, och minst hälften av dem är hormonellt inaktiva. [2]
Orsaker hypofysmikroadenom
Specialister känner inte till de exakta orsakerna till uppkomsten av ett mikroadenom i hypofysen - hjärnans endokrina körtel, vars celler producerar:
- kortikotropin eller ACTH -adrenokortikotropt hormon , som orsakar utsöndring av steroidhormoner av binjurebarken;
- tillväxthormon STH - somatotropt hormon ;
- gonadotropiner FSH - follikelstimulerande hormon och LH - luteiniserande hormon , som produktionen av kvinnliga könshormoner i äggstockarna och manliga könshormoner i testiklarna beror på;
- laktogent hormon prolaktin (PRL);
- tyreotropin eller sköldkörtelstimulerande hormon (TSH), som stimulerar syntesen av sköldkörtelhormoner.
Det antas att kraniocerebrala skador kan leda till uppkomsten av dessa neoplasmer; otillräcklig tillförsel av hypofysen med blod; cerebrala infektioner eller exponering för toxiner (som orsakar ödem och intrakraniell hypertoni).
Riskfaktorer
Det är känt att hypofysadenom och mikroadenom ofta förekommer i närvaro av en familjehistoria av MEN 1-syndrom - multipel endokrin adenomatos typ 1, som är ärftlig. Det finns alltså genetiskt bestämda riskfaktorer förknippade med vissa förändringar i DNA. [3]
Multipel endokrin neoplasi typ 4 (MEN4): MEN 4 har en mutation i genen för cyklinberoende kinashämmare 1B (CDKN1B), som orsakar hypofystumörer, hyperparatyreos, testikulära och cervikala neuroendokrina tumörer. [4]
Carney-komplex (CNC): Det finns en könscellsmutation i tumörsuppressorgenen PRKAR1A i Carney-komplexet som leder till primär pigmentär nodulär binjurebarksjukdom (PPNAD), testikeltumörer, sköldkörtelknölar, fläckvis hyperpigmentering av huden och akromegali. [5]
Den kliniska formen av familjär isolerade hypofysadenom (FIPA) kännetecknas av genetiska defekter i genen för arylkolvätereceptorinteragerande protein (AIP) i cirka 15 % av alla relaterade och 50 % av homogena somatotropinfamiljer.[6]
Familjärt isolerade hypofysadenom (FIPA): En mutation i det arylkolvätereceptorinteragerande proteinet (AIP) detekteras i tonåren eller tidig vuxen ålder i cirka 15 % av alla FIPA-fall. Dessa tumörer är vanligtvis aggressiva och utsöndrar oftast tillväxthormon, vilket orsakar akromegali.[7]
Möjligheten av förekomsten av denna typ av tumör på grund av funktionella störningar i andra endokrina körtlar och cerebrala strukturer, i synnerhet förändringar i det vaskulära systemet i hypotalamus , som inom det neuroendokrina hypotalamus-hypofyssystemet reglerar hypofysens arbete körtel och dess främre lob - adenohypofys, med dess frisättande hormoner, kan inte uteslutas.
Patogenes
Enligt dess histologi hänvisar hypofysadenom till godartade tumörer; beroende på storleken delas dessa neoplasier in i mikroadenom (upp till 10 mm i storlek på den bredaste punkten), makroadenom (10-40 mm) och jätteadenom (40 mm eller mer).
Genom att studera patogenesen av tumörbildning i hypofysen har det ännu inte varit möjligt att belysa mekanismerna för hyperplastisk transformation av cellerna i dess främre lob till en tumör.
Experter tror att en av de mest övertygande versionerna är sambandet med avregleringen av metabolismen av neurotransmittorn och hormonet dopamin (som är den huvudsakliga hämmaren av prolaktinsekretion) och / eller dysfunktionen hos de transmembrana dopaminreceptorerna i hypofyscellerna. Utsöndrar PRL (laktotrofer).
De flesta hypofysmikroadenom är sporadiska, men vissa förekommer som en del av genetiskt bestämda neuroendokrina syndrom som MEN 1-syndrom, McCune-Albrights syndrom, Werners syndrom, Carneys syndrom (eller Carney-komplex). I det senare fallet finns det en ökad risk att utveckla godartade tumörer i de hormonella (endokrina) körtlarna, inklusive hypofysen, binjurarna, sköldkörteln, äggstockarna och testiklarna.
Symtom hypofysmikroadenom
Ett hypofysmikroadenom kanske inte visar sig under mycket lång tid. Symtomen varierar beroende på plats och beror vanligtvis på endokrin dysfunktion. Detta är det vanligaste fyndet i fall av hormonell obalans i samband med överdriven produktion av ett eller flera hormoner. I de flesta fall, beroende på platsen, är detta ett mikroadenom i den främre hypofysen.
Det finns typer av hypofysmikroadenom beroende på deras hormonella aktivitet. Så den vanligaste typen anses vara ett icke-fungerande adenom - ett hormonellt inaktivt hypofysmikroadenom, som - tills det når en viss storlek - inte ger några symtom. Men ett växande hormonellt inaktivt hypofysmikroadenom kan komprimera närliggande hjärnstrukturer eller kranialnerver, så ett hypofysmikroadenom och en huvudvärk i frontala och temporala regionerna kan kombineras, [8]och synproblem är också möjliga. [9]Men enligt forskare är icke-fungerande (hormonellt inaktiva) hypofystumörer i 96,5 % av fallen makroadenom. [10]
Ett hormonellt aktivt hypofysmikroadenom (dess främre lob) kan också uppstå med ökad utsöndring av hormonet prolaktin- hypofys prolaktinom . Ökad produktion av PRL av laktotropa celler i adenohypofysen definieras som hyperprolaktinemi i hypofysmikroadenom.
Hur visar sig ett sådant mikroadenom i hypofysen hos kvinnor? En patologiskt hög nivå av detta hormon hämmar produktionen av östrogener, och de första tecknen manifesteras av menstruella oregelbundenheter - med frånvaro av menstruation (amenorré) och / eller deras ägglossningsfas. Som ett resultat utvecklas ihållande galaktorré-amenorrésyndrom och möjligheten till befruktning och graviditet går förlorad.
Ett prolaktinutsöndrande hypofysmikroadenom hos män kan leda till hyperprolaktinemisk hypogonadism med minskad libido, erektil dysfunktion, bröstförstoring (gynekomasti) och minskat hår i ansiktet och på kroppen.
Ett aktivt mikroödem som utsöndrar kortikotropin (ACTH) leder till ett överskott av steroidhormoner (glukokortikoider) som produceras av binjurebarken, vilket kan orsaka Itsenko-Cushings sjukdom av hypofysens etiologi.
Hos barn kan ett sådant mikroadenom manifestera sig med symtom på hyperkortisolism (Cushings syndrom), inklusive huvudvärk, allmän svaghet, överdriven avlagring av fettvävnad på bålen, minskad benmineraldensitet och muskelstyrka, randig hudatrofi (i form av lila striae), etc.
Med ett aktivt somatotropinproducerande mikroadenom ökar nivån av tillväxthormon i kroppen. I barndomen stimulerar dess överdrivna anabola effekt tillväxten av nästan alla kroppens ben och kan leda till gigantism; vuxna kan utveckla akromegali med ökad tillväxt av benen i ansiktets skalle (som orsakar en förvrängning av utseendet) och brosk i lederna i extremiteterna (vilket leder till en kränkning av deras proportioner och förtjockning av fingrarna), med ledvärk, överdriven svettning och utsöndring av talg, försämrad glukostolerans.
Mycket sällan (i 1-1,5 % av fallen) finns ett hypofysmikroadenom som producerar tyrotropin, och eftersom detta hormon har en stimulerande effekt på sköldkörteln har patienterna kliniska tecken på hypofyshypertyreos i form av sinustakykardi och förmaksflimmer, ökat blodtryck, viktminskning (med ökad aptit), samt ökad nervös excitabilitet och irritabilitet.
Det så kallade intrasellära hypofysmikroadenomet, en synonym - endosellärt hypofysmikroadenom, liksom hela hypofysen, är lokaliserat inom den turkiska sadeln (sella turcica) - inuti den anatomiska sadelformade fördjupningen i sfenoidbenet i skallbasen. I det här fallet är hypofysen belägen i botten av denna fördjupning - i hypofysens fossa (intrasellär region). Och hela skillnaden mellan termer är att "inuti" i lat. - intra och på grekiska. – endom.
Men ett hypofysmikroadenom med suprasellär tillväxt innebär att neoplasman växer uppåt från botten av hypofysen.
Cystiskt hypofysmikroadenom har en sluten säckliknande struktur och är asymptomatisk.
Hypofysmikroadenom med blödning kan vara resultatet av apoplexi eller hemorragisk infarkt i samband med förstoring av körteln och skada på de sinusformade kapillärerna i parenkymet i dess främre lob, neurohemala synapser och/eller portalkärl.
Hypofysmikroadenom och graviditet
Som redan nämnts är kvinnor med prolaktinproducerande hypofysmikroadenom - på grund av östrogenbrist och undertryckande av den pulserande utsöndringen av GnRH (gonadotropinfrisättande hormon) - vanligtvis infertila. För början av graviditeten är det nödvändigt att normalisera nivån av prolaktin, annars uppstår inte befruktning, eller så avslutas graviditeten i början.
- Är det möjligt att föda med hypofysmikroadenom?
Hos kvinnor med kliniskt fungerande mikroadenom som behandlas med dopaminagonister (kabergolin eller dostinex), kan prolaktinnivåerna återgå till normala och menstruationscykeln och fertiliteten kan återställas.
Är amning möjlig med hypofysmikroadenom?
Under postpartumperioden är amning tillåten i frånvaro av symtom på tumören, men det är nödvändigt att övervaka dess storlek (med hjälp av magnetisk resonanstomografi av hjärnan). Och om neoplasmen växer, stoppas amningen.
- Hypofysmikroadenom och IVF
Provrörsbefruktning kräver behandling av hyperprolaktinemi, och själva proceduren kan påbörjas om normala prolaktinnivåer är stabila i 12 månader och det inte finns några avvikelser i serumnivåerna av andra hypofyshormoner.
Komplikationer och konsekvenser
Varför är ett hypofysmikroadenom farligt? Även om denna tumör är godartad kan dess närvaro leda till komplikationer och konsekvenser, särskilt:
- leda till dysfunktion av hypotalamus-hypofys-binjuresystemet med utvecklingen av Itsenko-Cushings sjukdom;
- störa den hormonella regleringen av menstruationscykeln hos kvinnor och leda till erektil dysfunktion hos män;
- orsaka tillväxthämning och hypofysdvärgväxt (hypopituitarism) hos barn;
- provocera utvecklingen av osteoporos.
I fall av kompression av en växande tumör av fibrerna i de optiska nerverna i området för deras skärningspunkt (som hos 80 % av människorna är belägen direkt ovanför hypofysen), är det en kränkning av rörligheten hos ögon (oftalmoplegi) och en gradvis försämring av perifert syn. Även om mikroadenom vanligtvis är för små för att utöva sådant tryck.
Kan ett hypofysmikroadenom försvinna? Det kan inte lösa sig, men med tiden kan en hormonellt inaktiv tumör hos barn minska avsevärt. Men hos cirka 10 % av patienterna kan mikroadenom förstoras.
Diagnostik hypofysmikroadenom
För att diagnostisera ett hypofysmikroadenom krävs en fullständig patienthistoria och laboratorietester: blodprov för hormonnivåer (producerade av hypofysen), inklusive en radioimmunanalys av blodserum för prolaktinnivåer.
Om prolaktin är normalt med ett hypofysmikroadenom, är denna tumör hormonellt inaktiv. Men om det finns symtom på prolaktinom, kan ett sådant falskt negativt resultat vara resultatet av antingen ett laboratoriefel, eller så har patienten ett makroadenom som komprimerar hypofysstjälken.
Dessutom kan ytterligare tester krävas, till exempel för nivån av sköldkörtelhormoner (T3 och T4), immunglobuliner, interleukin-6 i blodserumet.
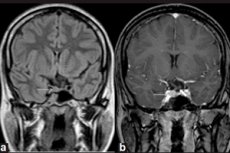
Endast instrumentell diagnostik med hjälp av magnetisk resonanstomografi (MRT) av hjärnan kan upptäcka ett mikroadenom . Och MRT i mikroadenom anses vara standarden för bildbehandling, med kontrastförstärkt MRT som har en känslighet på 90 %.
MR-tecken på ett hypofysmikroadenom inkluderar: volymen av körteln på sidan av mikroadenomet; en ökning av storleken på den turkiska sadeln; tunna ut och ändra konturen av dess botten (nedre väggen); lateral avvikelse av hypofysens tratt; isointensitet av det rundade området jämfört med grå substans i T1- och T2-viktade bilder; lätt hyperintensitet på T2-viktade bilder. [11]
Differentiell diagnos
Differentialdiagnos utförs med kraniofaryngiom, granulär celltumör (koristom) i hypofysen, Rathkes påsecysta, dermoidombildning, inflammation i hypofysen - autoimmun eller lymfocytisk hypofysit, feokromocytom, sköldkörtelsjukdomar, etc.
Hos kvinnor med en anovulatorisk cykel är hypofysmikroadenom och polycystiska äggstockar differentierade, eftersom 75-90% av fallen av bristande ägglossning är en konsekvens av polycystiskt ovariesyndrom .
Vem ska du kontakta?
Behandling hypofysmikroadenom
Med adenom och mikroadenom i hypofysen kan behandlingen vara medicinsk och kirurgisk. Samtidigt, om tumörerna är asymtomatiska, rekommenderas det att övervaka dem, det vill säga regelbundet genomföra MRI, för att inte missa början av deras ökning.
Syftet med det här eller det läkemedlet bestäms av vilken typ av neoplasm patienten har.
Farmakoterapi av PRL-utsöndrande tumörer utförs med läkemedel från gruppen av stimulatorer av dopamin D2-receptorer i hypotalamus (selektiva dopaminagonister), och de vanligaste är Bromocriptin (Parlodel, Bromergol), Norprolac och ett ergotderivat - Cabergolin eller Dostinex med hypofysmikroadenom med ökad utsöndring av prolaktin.
Biverkningar av Dostinex (kabergolin) kan innefatta en allergisk reaktion; huvudvärk och yrsel; illamående, kräkningar och buksmärtor; förstoppning; känner sig svag eller trött; sömnstörningar. Och bland biverkningarna av Bromocriptine (förutom en allergisk reaktion) noteras bröstsmärtor; snabba hjärtslag och andning med en känsla av brist på luft; hosta blod; försämrad koordination av rörelser m.m.
Läkemedlen Okreotid (Sandostatin), Lanreotid (Somatulin), Pegvisomant, som används för mikro- och makroadenom som utsöndrar tillväxthormon, tillhör STH-hämmare och antagonister av dess receptorer.
Och med ACTH-utsöndrande neoplasmer i adenohypofysen med Itsenko-Cushings syndrom, används Metyrapone (Metopirone) eller Mitotan (Lizodren).
Kirurgisk behandling bör övervägas för fungerande (hormonellt aktiva) mikroadenom. I fall där konservativ behandling är ineffektiv, och tumören kännetecknas av en lätt suprasellär expansion i den turkiska sadeln, kan en hypofysadenomektomi förskrivas - en operation för att avlägsna hypofysmikroadenomen. För närvarande utförs en transnasal eller transsfenoidal mikrodissektion, det vill säga avlägsnande av ett hypofysmikroadenom genom näsan.
Möjliga komplikationer och konsekvenser av avlägsnande av ett hypofysmikroadenom inkluderar postoperativ blödning och läckage av cerebrospinalvätska (ofta med behov av en andra operation), såväl som inflammation i hjärnhinnorna, synstörningar, hematombildning, övergående diabetes insipidus, återfall av mikroadenom.
Homeopati för hypofysmikroadenom med hyperprolaktinemi använder läkemedel vars verkan kan hjälpa till att delvis lindra symtomen. Till exempel, med oregelbunden menstruation och amenorré, ordineras ett botemedel från bläckfiskbläck Sepia och ett preparat från växten ängsryggvärk - Pulsatilla, och för galaktorré - ett botemedel baserat på europeisk cyklamenrot.
Uppenbarligen ska man inte hoppas att alternativ behandling för hypofysmikroadenom kan vara effektivare. Och inte bara för att med denna diagnos styrs örtläkare endast av klagomål från patienter (som inte vet om deras sanna etiologi), utan också på grund av opålitligheten hos många "folkmediciner". Du behöver inte leta långt efter exempel.
Vissa onlinekällor rekommenderar att du använder en blandning av vårprimula, ingefära och sesamfrö för att minska prolaktinnivåerna. Men primula hjälper bra med långvarig torrhosta, tunnare sputum och ingefärarötter, som sesamfrön, uppvisar laktogena egenskaper.
Du kan också hitta råd för att ta en tinktur av en fältbugg. Men i själva verket används detta botemedel internt för flatulens och externt för reumatiska ledsmärtor. Med all sannolikhet förväxlades vägglössen med rötterna av svart cohosh som användes mot värmevallningar under klimakteriet (dess andra namn är cimicifuga och black cohosh).
Näring för hypofysmikroadenom bör balanseras - med ett minskat socker- och saltintag. Detta är ingen specialdiet, utan helt enkelt en diet med lägre kalorier.
Alkohol är uteslutet med hypofysmikroadenom.
Vilken läkare ska jag kontakta med hypofysmikroadenom? Endokrinologer, gynekologer och neurokirurger hanterar de problem som uppstår med denna typ av tumör.
Förebyggande
Eftersom orsakerna till hypofystumörer relaterade till miljön eller livsstil är okända, kommer det helt enkelt inte att vara möjligt att förhindra utvecklingen av ett hypofysmikroadenom.
Prognos
De flesta hypofystumörer går att bota. Om ett hormonaktivt hypofysmikroadenom diagnostiseras i tid är chanserna till återhämtning stora och prognosen gynnsam.
Funktionshinder och hypofysmikroadenom: Funktionshinder kan vara förknippad med tumörtillväxt och skada på synnerven, såväl som andra konsekvenser av denna patologi, vars svårighetsgrad är individuell. Och erkännandet av en patient som en funktionshindrad person beror på de befintliga hälsorubbningarna och nivån av funktionsstörningar, som måste uppfylla juridiskt godkända kriterier.
Hypofysmikroadenom och armén: Patienter med denna tumör (även om den har tagits bort framgångsrikt) bör inte överhettas, stanna i solen under lång tid och fysiskt överanstränga sig. Så de är olämpliga för militärtjänst.
Hur länge lever människor med hypofysmikroadenom? Denna tumör är inte cancer, så det finns ingen gräns för förväntad livslängd. Även med ett aktivt GH-producerande mikroadenom kan patienter utveckla hypertoni och öka hjärtstorleken, och detta kan avsevärt minska deras förväntade livslängd. En ökad risk för dödsfall hos patienter äldre än 45 år noteras med Itsenko-Cushings sjukdom och akromegali.

