Medicinsk expert av artikeln
Nya publikationer
Goodpastures syndrom: orsaker, symtom, diagnos, behandling
Senast recenserade: 12.07.2025

Allt iLive-innehåll är mediekontrollerat eller faktiskt kontrollerat för att säkerställa så mycket faktuell noggrannhet som möjligt.
Vi har strikta sourcing riktlinjer och endast länk till välrenommerade media webbplatser, akademiska forskningsinstitut och, när det är möjligt, medicinsk peer granskad studier. Observera att siffrorna inom parentes ([1], [2] etc.) är klickbara länkar till dessa studier.
Om du anser att något av vårt innehåll är felaktigt, omodernt eller på annat sätt tveksamt, välj det och tryck på Ctrl + Enter.
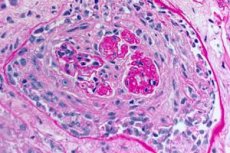
Goodpastures syndrom är ett autoimmunt syndrom som involverar alveolär lungblödning och glomerulonefrit orsakad av cirkulerande anti-GBM-antikroppar. Goodpastures syndrom utvecklas oftast hos individer med genetisk predisposition som röker cigaretter, men kolväteinandning och virusinfektioner i luftvägarna är möjliga ytterligare faktorer. Symtom på Goodpastures syndrom inkluderar dyspné, hosta, trötthet, hemoptys och/eller hematuri. Goodpastures syndrom misstänks hos patienter med hemoptys eller hematuri och bekräftas av närvaron av anti-GBM-antikroppar i blodet. Behandling av Goodpastures syndrom inkluderar plasmautbyte, glukokortikoider och immunsuppressiva medel såsom cyklofosfamid. Prognosen är god om behandlingen påbörjas innan andnings- eller njursvikt utvecklas.
Goodpastures syndrom beskrevs först av Goodpasture år 1919. Goodpastures syndrom är en kombination av glomerulonefrit och alveolär blödning i närvaro av antikroppar mot GBM. Goodpastures syndrom uppträder oftast som en kombination av diffus alveolär blödning och glomerulonefrit, men orsakar ibland isolerad glomerulonefrit (10–20 %) eller lungpåverkan (10 %). Män drabbas oftare än kvinnor.
Vad orsakar Goodpastures syndrom?
Orsaken till sjukdomen har inte exakt fastställts. En genetisk predisposition för Goodpastures syndrom antas, dess markör anses vara förekomsten av HLA-DRW2. Det finns en synvinkel på den möjliga rollen av en tidigare virusinfektion (hepatit A-virus och andra virussjukdomar), industriella risker och läkemedel (främst D-penicillamin).
Grunden för patogenesen av Goodpastures syndrom är bildandet av autoantikroppar mot basalmembranen i njurarnas och alveolernas glomerulära kapillärer. Dessa antikroppar tillhör IgG-klassen och binder till antikropparna i basalmembranen i närvaro av komplementkomponenten C3, vilket leder till en efterföljande utveckling av immuninflammation i njurarna och lungornas alveoler.
Anti-GBM-antikroppar riktas mot den icke-kollagena (NC-1) domänen i 3:e kedjan av typ IV-kollagen, vilken finns i högsta koncentration i basalmembranen i njur- och lungkapillärer. Exponering för miljöfaktorer - rökning, virala akuta respiratoriska infektioner och inandning av kolvätesuspensioner (oftare) - och, mer sällan, lunginflammation aktiverar presentationen av alveolära kapillärantigener till cirkulerande antikroppar hos personer med ärftlig predisposition (oftast är dessa bärare av allelerna HLA-DRwl5, -DR4 och -DRB1). Cirkulerande anti-GBM-antikroppar binder till basalmembran, fixerar komplement och inducerar ett cellulärt inflammatoriskt svar, vilket leder till utveckling av glomerulonefrit och/eller pulmonell kapillärit.
Det finns förmodligen en viss gemensamhet mellan autoantigener i basalmembranet i njurarnas och alveolernas glomerulära kapillärer. Autoantigenet bildas under inverkan av den skadliga effekten av den etiologiska faktorn. En okänd etiologisk faktor skadar och modifierar strukturen hos basalmembranen i njurarna och lungorna. Utsöndringen av de resulterande nedbrytningsprodukterna från njurarnas glomerulära basalmembran saktar ner och minskar när de skadas, vilket naturligt skapar förutsättningar för utveckling av autoimmuna skador på njurar och lungor. Det är fortfarande inte helt känt vilken komponent i basalmembranet som blir autoantigenet. För närvarande antas det att detta är den interna strukturella komponenten i njurarnas glomerulära basalmembran, a3-kedjan av typ 4-kollagen.
De bildade immunkomplexen avsätts längs basalmembranen i glomerulära kapillärer, vilket leder till utvecklingen av en immuninflammatorisk process i njurglomerulus (glomerulonefrit) och alveolerna (alveolit). De huvudsakliga cellerna som är involverade i utvecklingen av denna immuninflammation är T-lymfocyter, monocyter, endotelocyter, polymorfonukleära leukocyter och alveolära makrofager. Interaktionen mellan dem tillhandahålls av molekylära mediatorer, cytokiner (tillväxtfaktorer - trombocyter, insulinliknande, b-transformerande; interleukin-1, tumörnekrosfaktor, etc.). Arakidonsyrametaboliter, fria syreradikaler, proteolytiska enzymer och adhesiva molekyler spelar en viktig roll i utvecklingen av immuninflammation.
Aktivering av alveolära makrofager är av stor betydelse för utvecklingen av alveolit vid Goodpastures syndrom. I aktiverat tillstånd utsöndrar de cirka 40 cytokiner. Grupp I-cytokiner (kemotaxiner, leukotriener, interleukin-8) ökar flödet av polymorfonukleära leukocyter in i lungorna. Grupp II-cytokiner (tillväxtfaktorer - trombocyter, makrofager) främjar fibroblasters rörelse in i lungorna. Alveolära makrofager producerar också aktiva former av syre, proteaser, som skadar lungvävnaden.
Patomorfologi för Goodpastures syndrom
De huvudsakliga patomorfologiska manifestationerna av Goodpastures syndrom är:
- övervägande skador på njurarnas och lungornas mikrocirkulationssystem. I lungorna observeras en bild av venulit, arteriolit, kapillarit med uttalade fenomen av destruktion och proliferation; skador på kapillärerna observeras huvudsakligen i de interalveolära septa, alveolit med hemorragisk exsudat i alveolerna utvecklas. Njurskador kännetecknas av utveckling av extrakapillär proliferativ glomerulonefrit med efterföljande bildning av hyalinos och fibros, vilket leder till utveckling av njursvikt;
- uttalade intraalveolära blödningar;
- utveckling av pulmonell hemosideros och pneumoskleros av varierande svårighetsgrad, som ett resultat av utvecklingen av alveolit.
Symtom på Goodpastures syndrom
Sjukdomen uppvisar oftast kliniska manifestationer av lungpatologi. Hemoptys är det mest framträdande symptomet; hemoptys kan dock saknas vid hemorragiska manifestationer, och patienten kan endast uppvisa infiltrativa förändringar på lungröntgen eller med ett infiltrat och andnöd och/eller andningssvikt. Dyspné (främst vid ansträngning), hosta, sjukdomskänsla, minskad arbetsförmåga, bröstsmärtor, feber och viktminskning är vanliga. Upp till 40 % av patienterna har makrohematuri, även om lungblödning kan föregå njurmanifestationer med veckor till år.
Under hemoptys kan andnöden öka. Svaghet och minskad arbetsförmåga är också ett problem.
Symtomen på Goodpastures syndrom varierar över tid och sträcker sig från klara lungor vid auskultation till sprakande och torra rassel. Vissa patienter har perifert ödem och blekhet på grund av anemi.
Vid undersökning uppmärksammas blek hud, cyanos i slemhinnorna, pastositet eller uttalad svullnad i ansiktet, minskad muskelstyrka och viktminskning. Kroppstemperaturen är vanligtvis förhöjd till febernivåer.
Vid perkussion av lungorna kan en förkortning av perkussionsljudet konstateras över omfattande fokus på lungblödning, men detta observeras sällan; oftare sker inga förändringar i perkussionsljudet.
Ett karakteristiskt auskultatoriskt tecken på Goodpastures syndrom är torr och våt väsande andning, vars antal ökar avsevärt under eller efter hemoptys.
Vid undersökning av hjärt-kärlsystemet upptäcks arteriell hypertoni, eventuellt en ökning av gränsen för relativ hjärtslöhet åt vänster, dämpade hjärtljud, ett svagt systoliskt mumlande och perikardiellt friktionsmumlande uppträder vid utveckling av allvarlig njursvikt. Vid progressiv njurskada mot bakgrund av betydande arteriell hypertoni kan akut vänsterkammarsvikt med en bild av hjärtastma och lungödem utvecklas. Vanligtvis utvecklas denna situation i sjukdomens terminala skede.
Njurskador manifesterar sig som regel senare, efter en viss tid efter att lungsymtom utvecklats. Karakteristiska kliniska tecken på njurpatologi är hematuri (ibland makrohematuri), snabbt progredierande njursvikt, oliguri, arteriell hypertoni.
I 10-15% av fallen börjar Goodpastures syndrom med kliniska tecken på njurpatologi - den kliniska bilden av glomerulonefrit uppträder (oliguri, ödem, arteriell hypertoni, uttalad blekhet), och sedan ansluter sig symtom på lungskada. Många patienter kan ha myalgi, artralgi.
Oavsett debutvarianter är Goodpastures syndrom i de flesta fall allvarligt, sjukdomen fortskrider stadigt och svår lung- och njursvikt utvecklas. Patienternas förväntade livslängd från sjukdomsdebut varierar från flera månader till 1–3 år. Oftast dör patienterna av uremi eller lungblödning.
Vad stör dig?
Diagnos av Goodpastures syndrom
Diagnosen Goodpastures syndrom kräver detektion av serumanti-GBM-antikroppar genom indirekt immunofluorescens eller, när sådant är tillgängligt, genom direkt enzymlänkad immunosorbentanalys (ELISA) med rekombinant humant NC-1 α3. Andra serologiska tester, såsom antinukleära antikroppar (ANA), används för att detektera SLE och antistreptolysin-O-titer för att detektera poststreptokockglomerulonefrit, vilket kan vara orsaken till många fall av pulmonellt-renalt syndrom. ANCA är positiv (i perifera prover) i 25 % av fallen av Goodpastures syndrom. Njurbiopsi kan vara indicerat om glomerulonefrit föreligger (hematuri, proteinuri, röda blodkroppsslam vid urinanalys och/eller njursvikt). Snabbt progressiv fokal segmental nekrotiserande glomerulonefrit med ett progressivt förlopp finns vid biopsi vid Goodpastures syndrom och alla andra orsaker till pulmonellt-renalt syndrom. Immunofluorescensfärgning av njur- eller lungvävnad avslöjar klassiskt linjär deposition av IgG längs glomerulära eller alveolära kapillärer. Det ses också vid diabetisk njure och fibrillär glomerulonefrit, en sällsynt sjukdom som orsakar pulmonellt-njursyndrom, men detektion av GBM-antikroppar vid dessa sjukdomar är ospecifik.
Lungfunktionstester och bronkoalveolär lavage är inte diagnostiska för Goodpastures syndrom men kan användas för att bekräfta förekomsten av diffus alveolär blödning hos patienter med glomerulonefrit och lunginfiltrat men utan hemoptys. Lavagevätska som förblir hemorragisk efter flera tvättar kan bekräfta diffust hemorragiskt syndrom, särskilt om det finns en samtidig minskning av hematokrit.
 [ 3 ]
[ 3 ]
Laboratoriediagnostik av Goodpastures syndrom
- Allmän blodanalys. Karakteristiska drag är järnbristhypokrom anemi, hypokromi, anisocytos, poikilocytos av erytrocyter. Leukocytos, vänsterförskjutning av leukocytformeln och en signifikant ökning av ESR observeras också.
- Allmän urinanalys. Protein (graden av proteinuri kan vara betydande), cylindrar (granulära, hyalina, erytrocyter), erytrocyter (makrohematuri kan förekomma) finns i urinen. När kronisk njursvikt fortskrider minskar urinens relativa densitet och isohyposthenuri utvecklas i Zimnitsky-testet.
- Biokemiskt blodprov. Ökade blodnivåer av urea, kreatinin, haptoglobin, seromukoid, a2 och gammaglobuliner, minskat järninnehåll.
- Immunologiska studier. En minskning av antalet T-lymfocytsuppressorer kan detekteras, cirkulerande immunkomplex detekteras. Antikroppar mot basalmembranet i glomerulära och alveolära kapillärer detekteras med indirekt immunofluorescens eller radioimmunologiska metoder.
- Sputumanalys. Sputum innehåller många erytrocyter, hemosiderin och siderofager detekteras.
Instrumentell diagnostik av Goodpastures syndrom
- Röntgenundersökning av lungorna. Karakteristiska röntgentecken är lunginfiltrat i rotregionen som sprider sig till lungans nedre och mellersta delar, samt progressiva, symmetriska, bilaterala molnliknande infiltrat.
- Studie av den externa andningens funktion. Spirometri avslöjar en restriktiv typ av andningssvikt (minskad vitalkapacitet), allt eftersom sjukdomen fortskrider ansluter sig en obstruktiv typ av andningssvikt (minskat FEV1, Tiffeneau-index).
- EKG. Tecken på svår myokarddystrofi av anemisk och hypoxisk genes avslöjas (minskning av T-vågsamplituden och ST-intervallet i många avledningar, oftast i vänster bröstavledning). Vid svår arteriell hypertoni uppträder tecken på vänsterkammarmyokardhypertrofi.
- Blodgasanalys avslöjar arteriell hypoxemi.
- Undersökning av lung- och njurbiopsier. En biopsi av lungvävnaden (öppen biopsi) och njurarna utförs för slutgiltig verifiering av diagnosen om det är omöjligt att ställa en korrekt diagnos med icke-invasiva metoder. Histologisk och immunologisk undersökning av biopsierna utförs. Följande tecken är karakteristiska för Goodpastures syndrom:
- förekomsten av morfologiska tecken på glomerulonefrit (oftast extrakapillär), hemorragisk alveolit, hemosideros och interstitiell fibros;
- detektion av linjära avlagringar av IgG och komplementkomponent C3 på basalmembranen i lungalveolerna och njurglomerulerna med hjälp av immunofluorescensmetoden.
Diagnostiska kriterier för Goodpasture syndrom
Vid diagnos av Goodpastures syndrom är det lämpligt att använda följande kriterier.
- En kombination av lungpatologi och njurpatologi, dvs hemoptys (ofta lungblödning), andnöd och symtom på glomerulonefrit.
- Stadigt progressivt sjukdomsförlopp med utveckling av andnings- och njursvikt.
- Utveckling av järnbristanemi.
- Detektion under radiografisk undersökning av lungorna av flera bilaterala molnliknande infiltrat mot bakgrund av retikulär deformation av lungmönstret.
- Detektion i blodet av höga titrar av cirkulerande antikroppar mot basalmembranet i njurarnas glomeruli och alveoler.
- Detektion av linjära avlagringar av IgG och komplementkomponent C3 på basalmembranen i glomerulära och alveolära kapillärer.
- Avsaknad av andra systemiska (förutom pulmonella och njurmässiga) manifestationer.
Differentialdiagnos av Goodpastures syndrom
Goodpastures syndrom måste differentieras från ett antal sjukdomar som manifesteras av hemoptys eller lungblödning. Det är nödvändigt att utesluta onkologiska sjukdomar i bronker och lungor, tuberkulos, lungabscesser, bronkiektasi, hjärt- och kärlsjukdomar (vilket leder till nästäppa och hypertoni i lungcirkulationen), systemisk vaskulit, hemorragisk diates.
Screeningprogram för Goodpastures syndrom
- Allmänna blod- och urinprover.
- Biokemiskt blodprov: bestämning av totalt protein och proteinfraktioner, kreatinin och urea, transaminaser, seromukoid, haptoglobin, fibrin, järn.
- Sputumanalys: cytologisk undersökning, bestämning av siderofager.
- Immunologiska studier: bestämning av innehållet av B- och T-lymfocyter, subpopulationer av T-lymfocyter, immunglobuliner, cirkulerande immunkomplex, antikroppar mot basalmembranen i glomeruli i njurarna och alveolerna.
- Röntgenundersökning av lungorna.
- EKG.
- Spirometri.
- Undersökning av lung- och njurbiopsier.
Vilka tester behövs?
Behandling av Goodpastures syndrom
Behandling av Goodpastures syndrom inkluderar dagligt eller varannan dags plasmautbyte i 2 till 3 veckor (4 L plasmautbyte) för att avlägsna anti-GBM-antikroppar, i kombination med intravenösa glukokortikoider (vanligtvis metylprednisolon 1 g under minst 20 minuter varannan dag 3 gånger med prednisolon 1 mg/kg kroppsvikt dagligen) och cyklofosfamid (2 mg/kg en gång dagligen) i 6 till 12 månader för att förhindra bildandet av nya antikroppar. Behandlingen kan trappas ner när lung- och njurfunktionen upphör att förbättras. Långtidsmortalitet är relaterad till graden av njurfunktionsnedsättning vid sjukdomsdebut; patienter som behöver dialys tidigt och de med mer än 50 % halvmåneformade nefroner vid biopsi har överlevnadstider på mindre än 2 år och behöver ofta dialys om inte njurtransplantation övervägs. Hemoptys kan vara ett bra prognostiskt tecken eftersom det leder till tidigare upptäckt av sjukdomen; minoriteten av patienter som är ANCA-positiva svarar bättre på behandling för Goodpastures syndrom. Återfall förekommer i en liten andel av fallen och är förknippat med fortsatt rökning och luftvägsinfektion. Hos patienter med njursjukdom i slutstadiet som har genomgått en njurtransplantation kan sjukdomen återkomma i transplantatet.
Vad är prognosen för Goodpastures syndrom?
Goodpastures syndrom är ofta snabbt progredierande och kan vara dödligt om det inte diagnostiseras och behandlas omedelbart; prognosen är god när behandlingen påbörjas innan andnings- eller njursvikt utvecklas.
Omedelbar överlevnad vid tidpunkten för lungblödning och andningssvikt är förknippad med att säkerställa luftvägarnas öppenhet; endotrakeal intubation och mekanisk ventilation rekommenderas för patienter med gränsfall på arteriella blodgasnivåer och hotande andningssvikt.

