Medicinsk expert av artikeln
Nya publikationer
Myokardiell akinesi
Senast recenserade: 12.07.2025

Allt iLive-innehåll är mediekontrollerat eller faktiskt kontrollerat för att säkerställa så mycket faktuell noggrannhet som möjligt.
Vi har strikta sourcing riktlinjer och endast länk till välrenommerade media webbplatser, akademiska forskningsinstitut och, när det är möjligt, medicinsk peer granskad studier. Observera att siffrorna inom parentes ([1], [2] etc.) är klickbara länkar till dessa studier.
Om du anser att något av vårt innehåll är felaktigt, omodernt eller på annat sätt tveksamt, välj det och tryck på Ctrl + Enter.
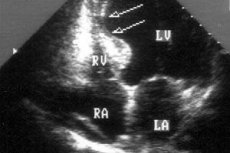
Vid diagnostisering av hjärtsjukdomar kan myokardiell akinesi detekteras, det vill säga dess immobilitet eller oförmågan hos vissa områden i hjärtmuskelvävnaden att dra ihop sig.
Således är myokardiell akinesi inte en sjukdom, utan ett patologiskt tillstånd, en störning av hjärtmuskelns normala motoriska funktion, vilket bestäms genom ultraljudsdiagnostik av hjärtat och är ett av de strukturella och funktionella tecknen på ett antal sjukdomar i hjärt-kärlsystemet.
Orsaker myokardiell akinesi
Varför slutar hjärtmuskeln att dra ihop sig, det vill säga, vilka är orsakerna till myokardiell akinesi?
Inom kardiologi är patogenesen av förlusten av normal kontraktil funktion i myokardiet (som, som bekant, utförs automatiskt av ett friskt hjärta) oftast förknippad med hjärtinfarkt och den resulterande nekrosen av en del av de fungerande kardiomyocyterna. Reparativa förändringar (ombyggnad) av myokardiet efter infarkt leder först till en ökning av infarktzonen, och sedan förvrängs och expanderas ventrikelns form, varvid kardiomyocytnekroszonen förvandlas till ett ärr och bildar ett område med myokardiell akinesi. Fibrösa förändringar kan också påverka septum som separerar ventriklarna, och då visar ultraljudsundersökning akinesi i området kring interventrikulära septum.
Hjärtinfarkt är ett akut tillstånd av hjärtischemi eller ischemisk hjärtsjukdom (IHD), som utvecklas när blodcirkulationen i kranskärlssystemet störs, vilket leder till hjärtmuskelhypoxi och celldöd.
Vid förtunning av hjärtats muskelmembran och dess utbuktning – aneurysm – efter infarkt visar ultraljudskardiografi akinesi i vänster kammare. Hos nästan två tredjedelar av patienterna uppstår aneurysmbildning i vänster kammare – på dess främre vägg eller vid apex, och här noteras även akinesi i hjärtats apex.
Dessutom finns det ett samband mellan ekokardiografiska resultat som visualiserar myokardiell akinesi och postinfarktiskt myokardsyndrom – fokal eller diffus postinfarktkardioskleros med karakteristisk ersättning av skadade kardiomyocyter med fibrös vävnad, samt med skador på hjärtats ledningssystem (nedsatt ledning av bioelektriska impulser från celler i sinoatriella eller atrioventrikulära lymfkörtlar).
I fall av myokarddegeneration eller dystrofi, som har en histomorfologisk bild som liknar kardioskleros, visar förändringar i hjärtmuskelvävnadens struktur också fokal myokardiell akinesi.
Ofta finns det skador på cellerna i sinusknutan med en minskning av muskelväggens rörelseamplitud och avsaknad av dess kontraktion, dvs. en kombination av hypokinesi och akinesi hos patienter med infektiös myokardit. Denna sjukdom kan åtföljas av bildandet av inflammatoriska infiltrat i interstitiet och lokaliserad myocytolys på grund av inflammation orsakad av virus (adeno- och enterovirus, Picornaviridae, Coxsackievirus, Parvovirus B, Rubellavirus, HSV-6), bakterier (Corynebacterium diphtheriae, Haemophilus influenzae, Borrelia burgdorferi, Mycoplasma pneumoniae), såväl som protozoer (Trypanosoma cruzi, Toxoplasma gondii), svampar (Aspergillus) eller parasiter (Ascaris, Echinococcus granulosus, Paragonimus westermani, etc.). Som klinisk statistik visar orsakas de flesta fallen av infektiös myokardit av difteri, influensa, enterovirus och toxoplasma.
Och med myokardit av autoimmun etiologi (associerad med systemisk lupus erythematosus, sklerodermi, reumatoid artrit, Whipples sjukdom, etc.) kan akinesi i vänster kammare och dess dysfunktion uppstå, fylld med livshotande arytmier.
Separat skiljer kardiologer mellan stresskardiomyopati (Takotsubo-kardiomyopati), som hushållsspecialister kallar brustet hjärtsyndrom. Denna plötsliga, övergående systoliska dysfunktion i vänster kammares mittapikala segment uppstår ofta i stressiga situationer hos äldre kvinnor som inte har en historia av kranskärlssjukdom. I synnerhet upptäcks en hyperkinesizon vid basen av vänster kammare, och ovanför den akinesi i hjärtats topp. Även vid ultraljud av hjärtat kan diagnostiker upptäcka en brist på rörelse i området kring interventrikulära septum.
Riskfaktorer
De viktigaste riskfaktorerna för störningar i hjärtmuskelområdenas normala motoriska funktion i form av myokardiell akinesi är utvecklingen av ischemisk hjärtsjukdom. Och riskfaktorerna för dess utveckling anses i sin tur vara:
- ålder över 45 år för män och över 55 år för kvinnor;
- familjehistoria av tidig hjärtsjukdom;
- minskade nivåer av kolesterolbärande HDL (högdensitetslipoproteiner) i blodet och ökade nivåer av lågdensitetslipoproteiner (LDL), vilka bidrar till avlagringar av kolesterol på blodkärlens väggar – ateroskleros;
- höga nivåer av triglycerider i blodet (relaterat till kosten);
- högt blodtryck;
- metabolisk störning (metaboliskt syndrom) som bidrar till ökat blodtryck och kolesterolavlagringar i kranskärlen;
- rökning (inklusive passiv rökning), fetma, brist på fysisk aktivitet, psykisk stress och depression.
Virala och bakteriella infektioner som påverkar hjärtmuskeln, liksom autoimmuna patologier, utlöser en sådan riskfaktor för myokardischemi som en ökning av nivån av C-reaktivt protein (CRP) i blodet. Och hjärtkärlens normala tillstånd störs av en obalans av vävnadsplasminogenaktivatorer (tPA) och deras hämmare (PAI), vilket utgör ett hot om trombos i kranskärlen med deras fullständiga ocklusion.
Patogenes
Det föreslås att patogenesen för denna kardiomyopati ligger i hjärtkärlens (kranskärl och/eller arterioler och kapillärer) otillräckliga reaktion på frisättningen av katekolaminneurotransmittorer i blodet, och att kortsiktiga avvikelser i hjärtmuskelkontraktionen uppstår på grund av den vasospasm de framkallar.
Symtom myokardiell akinesi
Vid myokardiell akinesi – ett ekokardiografiskt tecken på hjärt-kärlsjukdomar – bestäms den kliniska bilden av symtomen på dessa patologier. Bland dem finns: andnöd, smärta av varierande intensitet i hjärtområdet, arytmi (förmaks- eller ventrikulär), ventrikelfladder, svimning.
Således, med takotsubo-kardiomyopati, klagar patienter oftast på smärta bakom bröstbenet (av en klämmande natur) som strålar ut till vänster skulderblad och en känsla av brist på luft vid inandning.
Och smärtor vid myokardit kan vara både akuta och långvariga (utan effekt vid användning av nitroglycerin) och dämpade (klämande). Dessutom inkluderar hjärtsymtom vid denna sjukdom av infektiöst ursprung andnöd, feber, ökad hjärtfrekvens, hjärtfladder; blixtsnabba hemodynamiska störningar (en minskning av blodflödesvolymhastigheten), medvetslöshet och plötslig hjärtdöd är möjliga.
Komplikationer och konsekvenser
Myokardiell akinesi, jämfört med dyskinesi i ärrområdet efter infarkten, utgör visserligen en allvarligare livsfara för patienter med hjärtinfarkt. Studier har visat att i cirka 40 % av fallen av infarkt med koronarkärlsobstruktion, med snabb återställning av blodflödet i det ischemiska segmentet (reperfusion), kommer myokardiell kontraktilitet att återställas inom två till sex veckor efter infarkten. Konsekvenserna och komplikationerna inkluderar dock plötslig hjärttamponad, elektromekanisk dissociation och död.
Konsekvenserna och komplikationerna av dystrofiska förändringar i myokardiet med dess partiella akinesi leder till den nästan oundvikliga atrofin av muskelfibrer, vilket kan manifestera sig inte bara som arytmi och en minskning av systolisk utstötning, utan också som en expansion av hjärtkamrarna med kronisk cirkulationssvikt.
Vänsterkammarakinesi med dess systoliska dysfunktion och hjärtsvikt är bland de starkaste prediktorerna för risken för plötslig hjärtdöd.
 [ 23 ]
[ 23 ]
Diagnostik myokardiell akinesi
Endast instrumentell diagnostik av myokardiet med hjälp av ultraljudsundersökning av hjärtat – ekokardiografi – gör det möjligt att identifiera områden med dess akinesi.
En speciell metod för automatisk segmentanalys av hjärtkontraktioner möjliggör spårning och registrering av alla rörelser i hjärtväggen.
Vad behöver man undersöka?
Differentiell diagnos
Differentialdiagnos av bröstsmärta – hos patienter med en atypisk klinisk bild eller diagnostiskt obestämda elektrokardiogramresultat – innebär också användning av ekokardiografi.
Hos patienter utan hjärtmuskelstörning kan ekokardiografi användas för att upptäcka andra livshotande tillstånd med liknande klinisk bild: massiv lungemboli eller aortadissektion.
Dessutom inkluderar diagnostik av hjärtmuskeln, inklusive vid störningar i dess kontraktila funktion, blodprov för ESR, nivåer av C-reaktivt protein, antikroppar (serologisk analys av serum för IgM-nivåer), elektrolytnivåer och bestämning av markörer för hjärtmuskelskador (troponin I- och T-isoenzymer, kreatinkinas).
Patienter genomgår elektrokardiogram (EKG), röntgenkontrastbehandling av koronarangiografi, tomografisk scintigrafi (med radioisotopiska substanser), färgad vävnadsdoppler och MR. Diagnos av hjärtaneurysmer kräver användning av röntgenkontrastbehandling med ventrikulografi.
I vissa fall är differentialdiagnos av myokardiet endast möjlig med hjälp av endomyokardiell biopsi följt av histologi av det erhållna provet.
Vem ska du kontakta?
Behandling myokardiell akinesi
Behandling av hjärtmuskeln syftar till att återställa blodtillförseln till dess skadade områden (perfusion) och deras ledningsfunktion, begränsa området med lokaliserad kardiomyocytnekros och aktivera cellmetabolismen.
I klinisk praxis används läkemedel från flera farmakologiska grupper. Vid akuta koronarsyndrom och ocklusiv trombos i den epikardiella kransartären utförs reperfusionsbehandling med trombolytiska läkemedel (Streptokinas, Prourokinas, Alteplas) och trombocythämmande medel (Tiklopidin, Klopidogrelsulfat eller Plavix).
Vid kronisk hjärtsvikt används läkemedel som hämmar det angiotensinkonverterande enzymet (ACE) som reglerar blodtrycket: Captopril, Enalapril, Ramipril, Fosinopril. Doseringen bestäms av en kardiolog beroende på den specifika sjukdomen och EKG-mätningar. Till exempel kan Captopril (Capril, Alopresin, Tensiomin) förskrivas med 12,5-25 mg - tre gånger dagligen före måltid (oralt eller under tungan). Biverkningar av detta läkemedel och de flesta läkemedel i denna grupp inkluderar takykardi, blodtryckssänkning, njurfunktionsnedsättning, leversvikt, illamående och kräkningar, diarré, urtikaria, ökad ångest, sömnlöshet, parestesi och tremor, förändringar i blodets biokemiska sammansättning (inklusive leukopeni). Man bör komma ihåg att ACE-hämmare inte används vid idiopatiska hjärtmuskelpatologier, högt blodtryck, stenos i aorta och njurkärl, hyperplastiska förändringar i binjurebarken, ascites, graviditet och barndom.
Vid kranskärlssjukdom och kardiomyopati kan antiischemiska läkemedel i den perifera vasodilatorgruppen förskrivas, till exempel Molsidomin (Motazomin, Corvaton, Sidnofarm) eller Advocard. Molsidomin tas oralt - en tablett (2 mg) tre gånger om dagen; kontraindicerat vid lågt blodtryck och kardiogen chock; biverkning - huvudvärk.
Det antiarytmiska och blodtryckssänkande läkemedlet Verapamil (Veracard, Lekoptin) används vid kranskärlssjukdom med takykardi och angina: en tablett (80 mg) tre gånger dagligen. Biverkningar i form av illamående, muntorrhet, tarmproblem, huvudvärk och muskelsmärta, sömnlöshet, urtikaria och hjärtfrekvensrubbningar kan förekomma. Detta läkemedel är kontraindicerat vid svår hjärtsvikt, förmaksflimmer och bradykardi samt lågt blodtryck.
Läkemedlet Mildronat (Meldonium, Angiocardil, Vasonate, Cardionate och andra handelsnamn) har en kardiotonisk och antihypoxisk effekt. Det rekommenderas att ta en kapsel (250 mg) två gånger om dagen. Detta läkemedel kan endast användas av vuxna patienter och är kontraindicerat vid cerebrala cirkulationsstörningar och strukturella patologier i hjärnan. Vid användning av Mildronat är biverkningar som huvudvärk, yrsel, hjärtarytmi, andnöd, muntorrhet och hosta, illamående och tarmproblem möjliga.
Läkemedel i β1-adrenoblockergruppen för kranskärlssjukdom (Metoprolol, Propranolol, Atenolol, Acebutolol, etc.) sänker främst blodtrycket, och genom att minska sympatisk stimulering av receptorer på hjärtmuskelmembranen minskar de hjärtfrekvensen, minskar hjärtminutvolymen, ökar syreförbrukningen hos kardiomyocyter och lindrar smärta. Till exempel ordineras Metoprolol en tablett två gånger om dagen, Atenolol räcker med att ta en tablett per dag. Läkemedel i denna grupp ökar dock risken för akut hjärtsvikt och förmaks- och ventrikelblockad, och deras användning är kontraindicerad vid hjärtsvikt och dekompenserad hjärtsvikt, bradykardi och cirkulationsstörningar. Därför ifrågasätter många experter för närvarande den antiarytmiska effekten av dessa läkemedel.
Att lindra hjärtsmärta är av största vikt, eftersom sympatisk aktivering under smärta orsakar sammandragning av blodkärl och ökar belastningen på hjärtat. Nitroglycerin används ofta för att lindra smärta. Detaljerad information i artikeln - Effektiva piller som lindrar hjärtsmärta
Läkare rekommenderar att ta vitamin B6, B9, E, och för att stödja hjärtats retledningssystem – läkemedel som innehåller kalium och mangan (Panangin, Asparkam, etc.).
Kirurgisk behandling
Vid infarkter med skador på kranskärlen (vilket leder till bildandet av ett område med myokardischemi och dess akinesi med expansion av hjärtkamrarna) indikeras kirurgisk behandling för att återställa blodflödet till hjärtat - aortokoronär bypass.
Vid ischemisk hjärtsjukdom används koronardilatation (expansion av lumen) – stenting.
Kirurgisk behandling används oftast för dyskinetisk aneurysm: antingen genom aneurysmektomi (resektion), eller genom att suturera aneurysmhålan (aneurysmoplastik), eller genom att stärka dess vägg.
En metod för dynamisk kardiomyoplastik har utvecklats, vilken innebär att hjärtmuskelns kontraktilitet återställs eller förstärks med hjälp av elektriskt stimulerad skelettmuskulatur (vanligtvis en flik från kanten av latissimus dorsi-muskeln) lindad runt en del av hjärtat (med partiell resektion av det andra revbenet). Muskelfliken sys fast runt ventriklarna, och dess synkrona stimulering med hjärtkontraktioner utförs med hjälp av intramuskulära elektroder från en implanterbar hjärtpacemaker.
Förebyggande
Återgå till avsnittet om riskfaktorer, så blir metoderna för att förebygga kardiovaskulära patologier uppenbara. Det viktigaste är att inte gå upp i vikt, röra på sig mer och inte låta kolesterol sätta sig i form av plack på blodkärlens väggar, och för detta är det användbart efter 40 år (och förekomsten av hjärtsjukdomar hos blodsläktingar) att följa Dieten för åderförkalkning.
Och naturligtvis anser kardiologer att rökavvänjning är det viktigaste villkoret för att förhindra ischemisk skada på hjärtmuskeln. Faktum är att vid rökning kombineras hemoglobinproteinerna i de röda blodkropparna med gaserna från inandad tobaksrök och bildar en förening som är mycket skadlig för hjärtat - karboxyhemoglobin. Detta ämne hindrar blodkropparna från att transportera syre, vilket leder till hypoxi i hjärtmuskelns kardiomyocyter och utveckling av myokardischemi.
Läs också – Förebyggande av kardioskleros efter infarkt
Prognos
Kardiologer är ovilliga att ge prognostisk information: det är svårt att ställa en korrekt prognos för dyskinesi, hypokinesi och akinesi efter infarkt.
För att bedöma prognosen för dödlighet efter akut hjärtinfarkt introducerade experter från American Society of Echocardiography Wall Motion Index (WMI). Det har dock inte ett fullvärdigt långsiktigt prognostiskt värde.
När det gäller myokardit slutar nästan 30 % av fallen med återhämtning, enligt statistik, och i resten blir kronisk dysfunktion i vänster kammare en komplikation. Dessutom leder cirka 10 % av fallen av viral och mikrobiell myokardit till patientens död. Total akinesi i myokardiet leder till hjärtstillestånd.

