Medicinsk expert av artikeln
Nya publikationer
Ovariellt hyperstimuleringssyndrom
Senast recenserade: 05.07.2025

Allt iLive-innehåll är mediekontrollerat eller faktiskt kontrollerat för att säkerställa så mycket faktuell noggrannhet som möjligt.
Vi har strikta sourcing riktlinjer och endast länk till välrenommerade media webbplatser, akademiska forskningsinstitut och, när det är möjligt, medicinsk peer granskad studier. Observera att siffrorna inom parentes ([1], [2] etc.) är klickbara länkar till dessa studier.
Om du anser att något av vårt innehåll är felaktigt, omodernt eller på annat sätt tveksamt, välj det och tryck på Ctrl + Enter.
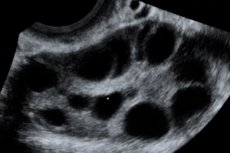
Ovariellt hyperstimuleringssyndrom (OHSS) är en iatrogen komplikation baserad på äggstockarnas hyperergiska, okontrollerade reaktion på administrering av gonadotropiner i ägglossningsstimuleringscykler och assisterad reproduktionsteknik.
Syndromet kan manifestera sig efter ägglossningsinduktion med klomifen eller vid graviditetens början i en spontan cykel.
 [ 1 ]
[ 1 ]
Epidemiologi
Incidensen av ovariellt hyperstimuleringssyndrom varierar från 0,5 till 14 % med olika ägglossningsstimuleringsscheman och tenderar inte att minska. Sjukdomen har varierande svårighetsgrad och kan vara dödlig på grund av utveckling av tromboemboliska komplikationer eller ARDS. Den förväntade dödligheten är 1 av 450–500 tusen kvinnor. Svåra former av syndromet, som kräver sjukhusvistelse på intensivvårdsavdelning, förekommer hos 0,2–10 %. Enligt det ryska nationella registret över assisterad reproduktionsteknik var incidensen av allvarligt ovariellt hyperstimuleringssyndrom år 2004 5,6 %.
Orsaker till ovariellt hyperstimuleringssyndrom
Riskfaktorer för att utveckla ovariellt hyperstimuleringssyndrom:
- ålder under 35 år,
- astenisk fysik,
- förekomsten av polycystiska eller multifollikulära äggstockar,
- mognad av fler än tio folliklar i ägglossningsstimuleringsprotokollet,
- användning av gonadotropinfrisättande hormonagonister och höga doser av gonadotropiner,
- graviditetens början,
- lutealfasstöd med hCG-preparat,
- allergiska sjukdomar.
Hur utvecklas ovariellt hyperstimuleringssyndrom?
Ovariellt hyperstimuleringssyndrom uppstår mot bakgrund av onormalt hög koncentration av könshormoner i blodplasman, vilket negativt påverkar funktionerna i olika kroppssystem, främst äggstockarna, och kännetecknas av en ökning av äggstockarnas storlek, ibland upp till 20-25 cm i diameter, med bildandet av follikulära och luteala cystor i dem mot bakgrund av uttalat stromalt ödem. Utlösaren för syndromets utveckling är administreringen av en ovulatorisk dos av koriongonadotropin. Utvecklingen av syndromet baseras på fenomenet "ökad vaskulär permeabilitet", vilket leder till en massiv frisättning av proteinrik vätska i det tredje utrymmet, interstitiet, och dess avsättning med utveckling av hypovolemi, hemokoncentration, oliguri, hypoproteinemi, elektrolytobalans, ökad aktivitet av leverenzymer, bildandet av ascites, hydrothorax, hydroperikardium med eller utan hypovolemisk chock. Emellertid är "faktor X" som orsakar vätsketransudation fortfarande okänd. I svåra fall uppstår anasarka, akut njursvikt, tromboemboliska komplikationer och ARDS.
För närvarande betraktas ovariellt hyperstimuleringssyndrom (OHSS) utifrån SIRS-syndrom (sjukdomar med ovariell hyperstimulering) (SIRS), mot bakgrund av vilket massiva skador på endotelet uppstår. Hos patienter med OHSS observerades höga koncentrationer av interleukiner (IL-1, IL-2, IL-6, IL-8), tumörnekrosfaktorer (TNF-α, TNF-(3)), vilka ökar syntesen av prostaglandiner av äggstockarna, ovariell neovaskularisering och vaskulär permeabilitet, i peritonealtransudatet. Under inverkan av proinflammatoriska cytokiner sker systemisk aktivering av koagulationsprocesser. Leukocytosens omfattning korrelerar med svårighetsgraden av SIRS. Organsystemiska skador vid OHSS liknar de skador som uppstår vid sepsis. Den mikrobiella faktorns roll vid OHSS och dess bidrag till utvecklingen av SIRS diskuteras för närvarande. Det antas att mikroorganismer som koloniserar tarmarna och urogenitalkanalen kan penetrera utanför deras livsmiljö och ha en effekt på kroppen som liknar den vid sepsis.
Symtom på ovariellt hyperstimuleringssyndrom
Syndromets svårighetsgrad är direkt relaterad till svårighetsgraden av de hemodynamiska störningar som orsakar den kliniska bilden. Syndromets uppkomst kan vara gradvis med ökande symtom eller plötslig (akut), där en kraftig omfördelning av vätska i kroppen sker inom några timmar med ansamling i serösa hålrum. När syndromet manifesteras uppstår klagomål om svaghet, yrsel, huvudvärk, flimrande "flugor" framför ögonen, andnöd i vila och vid fysisk ansträngning, torrhosta som intensifieras i liggande position, muntorrhet, illamående, kräkningar, diarré, uppblåsthet, en känsla av utspändhet, spänning, buksmärtor ofta utan tydlig lokalisering, sällsynt urinering, feber, svullnad av yttre könsorganen och nedre extremiteter.
Hos patienter med ovariellt hyperstimuleringssyndrom kan andningssvikt utvecklas på grund av begränsad lungrörlighet på grund av ascites, äggstocksförstoring eller pleurautgjutning. Förloppet av svårt OHSS i manifestationsstadiet kan kompliceras av akut hydrothorax, ARDS, lungemboli, lungemboli, atelektas och intraalveolär blödning. Pleurautgjutning diagnostiseras hos cirka 70 % av kvinnor med måttligt till svårt OHSS, och utgjutningen kan vara unilateral eller bilateral och uppträder mot bakgrund av ascites. Vid OHSS har förskjutning och kompression av mediastinumorganen på grund av massiv högersidig pleurautgjutning med utveckling av chock beskrivits, liksom dödlig utgång hos en kvinna med OHSS och hydrothorax på grund av atelektas, massiv blödning i alveollumen.
Hemodynamiska störningar. Vid måttlig och svår OHSS förekommer arteriell hypotoni och takykardi.
Ascites. Buken är utspänd, ofta spänd, smärtsam i alla områden, men oftare i hypogastrium i äggstockarnas projektion.
Njur- och leverdysfunktion. Urinretention, oliguri, anuri, hepatomegali observeras.
Förloppet av OHSS hos 80 % av patienterna med en svår form av syndromet åtföljs av feber. Hos 20 % av kvinnorna uppstår feber mot bakgrund av en urinvägsinfektion, hos 3,8 % - på grund av lunginflammation, hos 3,3 % - en övre luftvägsinfektion. Tromboflebit på grund av installation av en intravenös kateter orsakar feber hos 2 %, inflammation i det subkutana fettet vid punkteringsstället på bukväggen under laparocentes - hos 1 % av patienterna. Infektion av operationssåret förekommer hos 1 % och abscesser efter injektion (intramuskulär administrering av progesteron) hos 0,5 %. Feber av icke-infektiös genes hos varannan patient med OHSS är sannolikt förknippad med endogena pyrogena mekanismer. Isolerade fall av sepsis vid svår OHSS har beskrivits.
Mot bakgrund av syndromets utveckling inträffar en förvärring av latenta kroniska somatiska sjukdomar.
Vad stör dig?
Klassificering
Det finns ingen enskild klassificering av ovariellt hyperstimuleringssyndrom. Baserat på kliniska och laboratoriemässiga symtom urskiljs fyra svårighetsgrader av syndromet:
- Mild OHSS. Magbesvär, äggstockar upp till 8 cm i diameter med eller utan cystor, laboratorievärden är normala. Mild OHSS kallas "kontrollerad ovariell hyperstimulering", eftersom detta tillstånd observeras i absolut alla cykler av superovulationstimulering och för närvarande inte betraktas som ett patologiskt syndrom som kräver behandling.
- Måttlig OHSS. Måttlig smärta i alla delar av buken, illamående, kräkningar, diarré, äggstockar 8-12 cm i diameter med cystor, ultraljud och/eller kliniska tecken på ascites, hematokrit överstiger inte 45 %, leukocytos - 10-16x10 9 /l, hyperkoagulation (D-dimer - mer än 0,5 μg/ml, fibrinogenkoncentration - mer än 400 mg/dl, APTT, INR - inom normala gränser).
- Svårt OHSS. Hematokrit över 45 %, leukocytos 17–24 x 10 9 /l, hyperkoagulation (D-dimer över 5 μg/ml, fibrinogen över 600 mg/dl), äggstockar över 12 cm i diameter med cystor, alla kliniska och laboratoriemässiga tecken på måttligt OHSS och spänd ascites, hydrothorax, leverdysfunktion, oliguri [diures mindre än 0,5 ml/(kg h)].
- Kritisk OHSS. Hematokrit över 55 %, leukocytos över 25x109/l, spänd ascites, bilateral hydrothorax, hydroperikardium, anasarka, förstorade äggstockar upp till 20-25 cm, oliguri eller anuri, akut njursvikt, tromboemboliska komplikationer, ARDS.
Ovariellt hyperstimuleringssyndrom delas också in i tidigt och sent.
Om OHSS uppstår i lutealfasen och implantation inte sker, försvinner syndromet plötsligt och spontant med menstruationens början och når sällan en allvarlig form. Om implantation sker observeras oftast en försämring av patientens tillstånd under de första 12 veckorna av graviditeten. Sen OHSS orsakas av en signifikant ökning av hCG i blodplasman och är vanligtvis förknippad med implantation och tidig graviditet.
Konsekvenser och komplikationer
Komplikationer av ovariellt hyperstimuleringssyndrom kan fortsätta med utvecklingen av tromboemboliska komplikationer. Orsaken till trombos vid OHSS är fortfarande okänd, men huvudrollen i patogenesen av detta tillstånd tillskrivs höga koncentrationer av könshormoner, proinflammatoriska cytokiner, hemokoncentration och en minskning av venöst kärl (VCP). Långa sjukhusvistelser, begränsad motorisk aktivitet, minskat venöst återflöde på grund av en ökning av äggstockarna, en ökning av aktiviteten hos koagulationsfaktorer, fibrinolyshämmare och trombocyter bidrar ytterligare till den höga risken för att utveckla trombotiska komplikationer i samband med OHSS. Det har visats att hos 84 % av patienterna med tromboemboliska komplikationer som uppstod efter ägglossningsinduktion och i assisterad reproduktionsteknik, skedde deras utveckling mot bakgrund av graviditeten. I 75 % av fallen noterades trombbildning i venbädden med en dominerande lokalisering i kärlen i övre extremiteter, nacke och huvud (60 %). Ett antal patienter diagnostiserades med spontan arteriell trombos lokaliserad i hjärnkärlen. Mer sällan observerades tromber i femorala, popliteala, carotis-, subclavia-, iliaca-, ulnara-, mesenteriala artärer och aorta. Litteraturen presenterar en observation av utvecklingen av ocklusion av den centrala retinala arterien med synförlust vid OHSS. Incidensen av lungemboli hos patienter med OHSS och djup ventrombos i nedre extremiteterna är 29 %, medan risken för denna komplikation hos kvinnor med OHSS och djup ventrombos i övre extremiteterna och arteriell trombos är signifikant lägre och är 4 respektive 8 %.
Svåra fall av ovariellt hyperstimuleringssyndrom kan åtföljas av komplikationer som kräver kirurgiskt ingrepp - bristning av en äggstockscysta och intraabdominell blödning, torsion av livmoderbihangen, utomkvedshavandeskap.
Diagnos av ovariellt hyperstimuleringssyndrom
Diagnosen ovariellt hyperstimuleringssyndrom ställs utifrån anamnesdata, en omfattande klinisk, laboratorie- och instrumentell undersökning som avslöjar förstorade äggstockar med multipla cystor, uttalad hemokoncentration och hyperkoagulation hos en patient som använt assisterad reproduktionsteknik eller kontrollerad ägglossningsinduktion under denna cykel för att uppnå graviditet.
Laboratorieforskning
Kliniskt blodprov
Hematokrit över 40 %, hemoglobinkoncentration över 140 g/l, leukocytos upp till 50x10 9 /l utan vänsterförskjutning, trombocytos upp till 500-600x10 6 /l. Hemokoncentration (hematokrit över 55 %) indikerar ett potentiellt hot mot livet.
Biokemiskt blodprov
Elektrolytobalans, inklusive hyperkalemi (mer än 5,3 mmol/l) och hyponatremi (mer än 135 mmol/l), vilket leder till minskad plasmaosmolaritet. Hypoproteinemi (totalt protein mer än 66 g/l), hypoalbuminemi (albumin mindre än 35 g/l), högt C-reaktivt protein, förhöjda levertransaminaser upp till 800 U/l, i vissa fall förhöjt GGT eller alkaliskt fosfatas, hos vissa patienter - förhöjd kreatininkoncentration mer än 80 μmol/l och urea mer än 8,3 mmol/l.
 [ 20 ], [ 21 ], [ 22 ], [ 23 ]
[ 20 ], [ 21 ], [ 22 ], [ 23 ]
Koagulogram
Ökade fibrinogennivåer över 400 mg/dl, von Willebrands faktor över 140 %, minskade antitrombin III-koncentrationer under 80 %, D-dimer över 0,5 mcg/ml. Normala värden för APTT, PTI, INR.
 [ 24 ]
[ 24 ]
Blodimmunglobuliner
Minskad koncentration av IgG och IgA i blodplasma. Allmän urinanalys. Proteinuri.
Analys av ascitisk vätskas sammansättning
Högt proteininnehåll (mer än 42 g/l) och albumin (mer än 23 g/l), lågt antal vita blodkroppar, relativt högt antal röda blodkroppar, höga koncentrationer av alla proinflammatoriska cytokiner, C-reaktivt protein upp till 135 mg/l (normalt 0-8,2 mg/l), globulinfraktion av proteiner.
 [ 25 ], [ 26 ], [ 27 ], [ 28 ], [ 29 ], [ 30 ], [ 31 ]
[ 25 ], [ 26 ], [ 27 ], [ 28 ], [ 29 ], [ 30 ], [ 31 ]
Tumörmarkörer i blodplasma
Koncentrationen av CA-125, som återspeglar massiv proliferation av äggstocksvävnad, når sina maximala värden (upp till 5125 U/ml) vid den andra veckan av OHSS-utveckling, när båda äggstockarna är som mest förstorade. Den förhöjda nivån av tumörmarkören kvarstår i upp till 15–23 veckor efter att tecken på ovariellt hyperstimuleringssyndrom uppstått, trots behandlingen.
Procalcitonin i blodserum bestäms hos 50 % av patienterna i intervallet 0,5–2,0 ng/ml, vilket betraktas som en måttlig systemisk inflammatorisk reaktion.
Mikrobiologisk forskning
Vid undersökning av urin som utsöndras från slidan och livmoderhalskanalen isoleras atypiska patogener Pseudomonas, Proteus, Klebsiella, Enterobacter, E. coli i mängder på mer än 10 000 CFU/ml.
Instrumentell forskning
Ultraljud av bäckenorganen
Förstorade äggstockar från 6 till 25 cm i diameter med flera cystor, normal eller förstorad livmoder, förekomst av fri vätska i bäckenhålan och normal progressiv singel- eller flergraviditet.
Ultraljud av bukorganen
Närvaron av fri vätska i bukhålan i en mängd av 1 till 5-6 liter. Normal leverstorlek och struktur eller hepatomegali. Ekotecknen på gallvägsdyskinesi. Vid undersökning av njurarna är calyceal-bäckenkomplexet oförändrat.
Ultraljud av pleurahålorna
Förekomst av fri vätska i ekokardial sfär (ECOCG). Mot bakgrund av hemodynamiska störningar, minskad EF, minskad slutdiastolisk volym, minskat venöst återflöde, i vissa fall - förekomst av fri vätska i perikardialhålan.
EKG
Rytmstörningar såsom ventrikulär extrasystoli, takykardi, diffusa metabola och elektrolytförändringar i myokardiet. Lungröntgen. Utförs vid misstanke om ARDS och tromboembolism. Ett karakteristiskt röntgenfynd vid ARDS är uppkomsten av ett "slipat glas"-mönster och diffusa multifokala infiltrat med ganska hög densitet (konsolidering) med väldefinierade luftbronker, dvs. utveckling av omfattande skador på lungparenkymet. Vid lungemboli avslöjar röntgenbilden en hög position av diafragmakupolen, diskoid atelektas, pletora av en av lungrötterna eller en "avskuren" rot, utarmning av lungmönstret över lungans ischemiska område och en perifer triangulär inflammationsskugga.
Indikationer för samråd med andra specialister
På grund av att alla organ och system är involverade i den patologiska processen är en undersökning av en terapeut obligatorisk. Vid misstanke om trombotiska komplikationer krävs en konsultation med en kärlkirurg. Vid uttalad hydrothorax krävs en konsultation med en thoraxkirurg för att besluta om pleurapunktion.
Vad behöver man undersöka?
Hur man undersöker?
Vilka tester behövs?
Behandling av ovariellt hyperstimuleringssyndrom
Avsaknaden av en tydlig uppfattning om patofysiologin för ovariellt hyperstimuleringssyndrom (OHSS) gör det omöjligt att genomföra effektiv, patogenetiskt underbyggd behandling som effektivt och snabbt stoppar utvecklingen av syndromet och flera organsjukdomar som åtföljer svåra former av ovariellt hyperstimuleringssyndrom. För närvarande finns det ingen specifik behandling för ovariellt hyperstimuleringssyndrom, så behandlingsåtgärderna för dessa patienter reduceras till patogenetisk terapi tills spontan regression av syndromet sker då koncentrationen av hCG i blodplasman minskar under 7 dagar i cykler där graviditet inte har inträffat, eller 10-20 dagar när graviditet har inträffat. De flesta patienter som är inlagda på intensivvårdsavdelningar läggs redan in med diagnosen OHSS efter öppenvårdsbehandling, som består av daglig bedömning av vikt och diures, begränsning av överdriven fysisk aktivitet och sexuell aktivitet, rikligt drickande med tillsats av lösningar rika på elektrolyter och regelbundna blodprover. Diskussionen om behandlingsstrategin för denna patientgrupp innefattar omfattande symptomatisk behandling som syftar till att förhindra utvecklingen av PRF genom att återställa CCP, eliminera hemokoncentration, elektrolytubalans, förebygga akut njursvikt, ARDS och tromboemboliska komplikationer.
Steg 1 - bedömning av tillståndets svårighetsgrad
Det första steget i att bestämma taktiken för att behandla en patient med ovariellt hyperstimuleringssyndrom är att bedöma hemodynamiken och andningsfunktionen. Det är också nödvändigt att genomföra en fullständig fysisk undersökning med en grundlig studie av tillståndet i extremiteter, huvud och nacke för att utesluta djup ventrombos och installera en perifer venkateter eller central venkateterisering. Subklaviavenkateterisering är mest lämpligt, eftersom risken för trombos i detta fall är den lägsta. Kateterisering av urinblåsan är nödvändig för att bedöma diuresen. Det är nödvändigt att undersöka kliniska blodprovsparametrar, blodplasmaelektrolyter, protein, leverenzymaktivitet, kreatinin, ureanivåer och koagulogramparametrar dagligen. Ultraljud av buken utförs för att bestämma graden av äggstocksförstoring och förekomsten av ascites.
Steg 2 - infusionsbehandling
Läkemedelsbehandling av patienter med OHSS bör inriktas på att upprätthålla hemodynamiken och mobilisera vätska i bukhålan genom att skapa en negativ natrium- och vattenbalans. Det primära målet är att ersätta volymen av cirkulerande vätska för att minska hemokoncentrationen och upprätthålla tillräcklig njurfiltration. Kristalloida och kolloida lösningar används för infusionsbehandling av ovariellt hyperstimuleringssyndrom.
Valet av kristalloidlösning bestäms av elektrolytobalansen. Vid bestämning av mängden administrerade kristalloider är det nödvändigt att beakta att vid generell endotelskada bör volymen av dessa lösningar vara 2-3 gånger mindre än volymen av kolloidlösningar, eftersom övervikt av kristalloider förvärrar vätskeansamling i serösa hålrum och i vissa fall leder till utveckling av anasarka.
Det föredragna läkemedlet för återställning och bibehållande av intravaskulär volym hos patienter med OHSS är hydroxietylstärkelse 130/0 42 daglig volym - 25-30 ml/kg. Hydroxietylstärkelse 200/0 5 kan också användas i grundbehandlingen av OHSS i en volym av 20 ml/(kg x dag). Det kan dock ansamlas i kroppen och vid långvarig användning kan det orsaka leverdysfunktion och öka nivån av levertransaminaser, ibland upp till 800 U/l. Hos denna patientgrupp är det olämpligt att använda hydroxietylstärkelse 450/0 7 på grund av den höga risken för allergiska reaktioner, negativ inverkan på njur- och leverfunktion, försämring av hemokoagulationsparametrar (förlängning av blodets koagulationstid, risk för hemorragiska komplikationer). Indikationer för användning av dextranlösningar begränsas av den höga frekvensen av allergiska reaktioner, negativ påverkan på hemostassystemet, frisättning av von Willebrands faktor, induktion av den proinflammatoriska kaskaden och avsaknaden av påverkan på blodets reologiska egenskaper i de doser som används. Infusion av dextraner under förhållanden med ökad kapillärpermeabilitet kan leda till utveckling av det så kallade dextransyndromet, åtföljt av OL, nedsatt lever- och njurfunktion och utveckling av koagulopati. Gelatinlösningar är inte heller avsedda för infusionsbehandling vid OHSS.
Vid hypoproteinemi mindre än 25 g/l används en 20-procentig albuminlösning, den dagliga volymen är 3 ml/kg. Det rekommenderas att endast använda en 20-procentig albuminlösning, eftersom det onkotiska trycket för en 20-procentig lösning är cirka 100 mm Hg, och det onkotiska trycket för en 5-procentig lösning är cirka 20 mm Hg. Under förhållanden med hög permeabilitet i det vaskulära endotelet leder infusion av en 5-procentig albuminlösning, i motsats till en 20-procentig lösning, till ett mer intensivt utbyte med den extravaskulära poolen och en kraftig ökning av det onkotiska trycket i interstitiet, vilket leder till en ökning av interstitiell hyperhydrering av lungorna.
Diuretika är motiverade vid oliguri, perifert ödem, som når hematokritvärden på 36-38 %. För tidig eller överdriven förskrivning av diuretika kan förvärra hypovolemi och hemokoncentration, vilket ökar risken för trombotiska komplikationer. Furosemid används huvudsakligen - 20-40 mg en gång intramuskulärt eller intravenöst långsamt i 1-2 minuter.
Principer för infusionsbehandling vid ovariellt hyperstimuleringssyndrom
Efter att den initiala dosen av kristalloid- och kolloidlösningar har administrerats bestäms volymen för ytterligare infusionsbehandling med hänsyn till följande parametrar: diures - mindre än 1 ml/(kg h), hematokrit mindre än -40 %, medelartärtryck - mer än 70 mm Hg, centralt ventryck - 8–10 mm H2O. När de angivna parametrarna har uppnåtts avbryts infusionsbehandlingen. Det är lämpligt att administrera den totala dagliga volymen infusionslösningar i fraktioner under dagen. Underlåtenhet att följa dessa metoder leder till utveckling av hemodilution, vilket framkallar snabb vätskeansamling i serösa hålrum och försämring av patientens tillstånd. Ett typiskt misstag vid behandling av kvinnor med OHSS är den oberättigade förlängningen av infusionsbehandlingen när hemodynamiska parametrar har normaliserats och ett försök att helt stoppa utvecklingen av OHSS som ett iatrogent tillstånd.
Steg 3 - förebyggande av komplikationer
Förebyggande av trombos och tromboembolism
Grunden för att förebygga trombotiska komplikationer vid ovariellt hyperstimuleringssyndrom är att eliminera hemokoncentration. Antitrombotisk behandling är indicerad när laboratorietecken på hyperkoagulation uppträder. LMWH används för detta:
- kalciumnadroparin (daglig dos - 100 anti-Xa IE/kg 2 gånger subkutant),
- dalteparinnatrium (100–150 anti-Xa IE/kg 2 gånger subkutant),
- enoxaparinnatrium (1 ml/kg/dag) 1–2 gånger subkutant).
Laboratorieövervakning - bestämning av plasma-anti-Xa-aktivitet 3 timmar efter administrering av LMWH, vilket möjliggör upprätthållande av en effektiv dos av läkemedlet inom det säkra terapeutiska intervallet och därmed minimerande av sannolikheten för blödning. Antitrombotiska läkemedel fortsätter tills blodkoagulationsparametrarna är normaliserade. Övervakning utförs genom att bestämma koncentrationen av D-dimer i plasma med hjälp av en kvantitativ metod. Varaktigheten av LMWH-administrering bestäms individuellt och kan i vissa fall överstiga 30 dagar.
Förebyggande av infektiösa komplikationer
Med tanke på den positiva effekten av att förskriva immunglobulinpreparat för att förebygga sekundära infektioner vid andra sjukdomar som åtföljs av proteinförlust, kan man förvänta sig effektiviteten av denna behandling hos patienter med OHSS. För att slutgiltigt bekräfta eller vederlägga denna hypotes ur evidensbaserad medicinsynpunkt är det dock nödvändigt att genomföra studier. För närvarande är indikationen för empirisk antibakteriell behandling risken för sekundär infektion hos patienter i kritiskt tillstånd eller med instabil hemodynamik. Det empiriskt valda läkemedlet ändras baserat på resultaten av bakteriologiska tester. Vid förskrivning av empirisk antibakteriell behandling är det nödvändigt att vägledas av information om sjukdomens svårighetsgrad, riskfaktorer för infektion och egenskaperna hos antibiotikaresistens på en given intensivvårdsavdelning.
Näringsstöd
Det administreras per os till alla patienter med allvarlig och kritisk OHSS. Det är nödvändigt att följa rekommendationerna:
- energivärde 25–35 kcal/(kgxdag),
- glukos - mindre än 6 g/(kg x dag),
- lipider - 0,5–1 g/(kg x dag),
- proteiner - 1,2–2 g/(kg x dag),
- standard daglig uppsättning av mikroelement och vitaminer.
Steg 4 - kirurgiska metoder
Indikationer för laparocentes hos kvinnor med ovariellt hyperstimuleringssyndrom:
- progressiv spänd ascites,
- oliguri mindre än 0,5 ml/dkg/min),
- en ökning av kreatininkoncentrationen över 80 μmol/l eller en minskning av dess clearance,
- hemokoncentration med ett hematokritvärde på mer än 40%, inte mottaglig för läkemedelskorrigering.
Transabdominal eller transvaginal åtkomst kan väljas för laparocentes. Förstorade äggstockar skapar tekniska svårigheter, varför användning av ultraljudskontroll är extremt viktig. Långtidsdränering av bukhålan (transabdominal laparocentes) från 14 till 30 dagar med portionsvis avlägsnande av peritonealt transudat med apyrogen cystoFix®-kateter har ett antal fördelar, eftersom det gör det möjligt att undvika engångsevakuering av en stor volym peritonealt transudat och därigenom eliminera kraftiga fluktuationer i det intraabdominella trycket som orsakar hemodynamiska störningar, stabilisera patientens tillstånd och undvika upprepade punktioner av bukhålan för att avlägsna ascitesvätska hos denna patientkategori. Den totala volymen evakuerad ascitesvätska under behandling av svår OHSS kan variera från 30 till 90 liter.
Hos patienter med hydrothorax mot bakgrund av ovariellt hyperstimuleringssyndrom är en avvaktande strategi motiverad. När hydrothorax bildas utförs en punktering av pleurahålan endast vid allvarlig progressiv andningssvikt.
Kriterier för initiering av andningsstöd vid svårt och kritiskt ovariellt hyperstimuleringssyndrom:
- brist på spontan andning och patologiska andningsrytmer,
- minskning av andningsindex till mindre än 200 mm Hg,
- livshotande hjärtrytmrubbningar,
- ihållande takykardi över 120,
- svår hypotoni,
- takypné över 40,
- involvering av accessoriska andningsmuskler.
Vid utveckling av ARDS och överföring till mekanisk ventilation används följande:
- små andningsvolymer (6 ml/kg),
- inspirationstryck <30 cm H2O,
- PEEP (>10 cm H2O),
- Den alveolära rekryteringsmanövern används.
Kirurgisk behandling av ovariellt hyperstimuleringssyndrom är endast motiverad vid akut patologi av bihangsvridning, ruptur av äggstockscystan eller blödning från äggstockscystan. Vid äggstocksvridning är laparoskopisk uppvridning av äggstocken mest effektiv. Ett typiskt misstag i behandlingsstrategin för patienter med okomplicerad ovariell hyperstimuleringssyndrom är akut kirurgi och resektion av cirka 30-50% av äggstocksvävnaden eller bilateral ooforektomi.

