Medicinsk expert av artikeln
Nya publikationer
Hjärtkateterisering
Senast recenserade: 06.07.2025

Allt iLive-innehåll är mediekontrollerat eller faktiskt kontrollerat för att säkerställa så mycket faktuell noggrannhet som möjligt.
Vi har strikta sourcing riktlinjer och endast länk till välrenommerade media webbplatser, akademiska forskningsinstitut och, när det är möjligt, medicinsk peer granskad studier. Observera att siffrorna inom parentes ([1], [2] etc.) är klickbara länkar till dessa studier.
Om du anser att något av vårt innehåll är felaktigt, omodernt eller på annat sätt tveksamt, välj det och tryck på Ctrl + Enter.
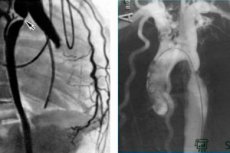
Kateterisering av hjärthålorna utförs med hjälp av punktering och perkutan insättning av en kateter i ett kärl - en perifer ven (ulnar, subclavia, jugular, femoral) för hjärtets högra kammare eller en artär (brachial, femoral, axillär, radial) för hjärtets vänstra kammare.
Metod för att utföra hjärtkateterisering
Vid kraftig förträngning av aortaklaffen eller dess artificiella protes, när det är omöjligt att retrogradt föra in en kateter i vänster kammare, används en transseptal punktering av det interatriella septumet från höger förmak till vänster och sedan in i vänster kammare. Den vanligaste metoden för att nå kärlet är enligt Seldinger-metoden (1953). Efter lokalbedövning av hud och subkutan vävnad med 0,5-1% novokainlösning eller 2% lidokainlösning och ett litet skåra på huden, punkteras en ven eller artär med en nål; när blod kommer ut från nålens proximala spets (paviljong) (det är nödvändigt att försöka punktera endast kärlets främre vägg), förs en styrtråd genom nålen, nålen tas bort och en kateter förs in i kärlet längs styrtråden, som naturligtvis bör vara längre än katetern. Katetern förs fram till önskad plats under röntgenkontroll. Vid användning av flytande katetrar av Swan-Gans-typen med en ballong i änden bestäms kateterspetsens placering av tryckkurvan. Det är att föredra att installera en tunnväggig introducer med en hemostatisk ventil och en sidogren för spolning in i kärlet, och genom den är det enkelt att föra in katetern och ersätta den med en annan vid behov. Katetern och introducern tvättas med hepariniserad isoton natriumkloridlösning för att förhindra trombbildning. Med hjälp av olika typer av katetrar är det möjligt att nå olika delar av hjärtat och kärlen, mäta trycket i dem, ta blodprover för oximetri och andra tester, föra in RVC för att bestämma anatomiska parametrar, förträngningar, blodutsöndring etc.
Om det inte finns någon fluoroskopisk (röntgen) kontroll över kateterns placering används katetrar med en uppblåsbar flytande ballong i änden, som kan röra sig med blodflödet in i höger förmak, höger kammare, lungartären och registrera trycket i dem. Lungartärens kiltryck möjliggör indirekt bedömning av vänster kammares funktion, dess slutdiastoliska tryck (EDP), eftersom vänster kammares EDP är det genomsnittliga trycket i vänster förmak eller trycket i lungkapillärerna. Detta är viktigt för övervakning av behandling vid hypotoni, hjärtsvikt, till exempel vid akut hjärtinfarkt. Om katetern har ytterligare anordningar är det möjligt att mäta hjärtminutvolymen med hjälp av färgämnesutspädning eller termodilution, registrera ett intrakavitärt elektrogram och utföra endokardiell stimulering. De intrakavitära tryckkurvorna registreras med hjälp av en Statham vätsketrycksensor och ett EKG på en jet-inspelare eller dator med möjlighet till utskrift på papper; deras förändringar kan användas för att bedöma en specifik hjärtpatologi.
Mätning av hjärtminutvolym
Det bör noteras att det inte finns några absolut exakta metoder för att mäta hjärtminutvolymen. Vid hjärtkateterisering används oftast tre metoder för att bestämma hjärtminutvolymen: Fick-metoden, termodilutionsmetoden och den angiografiska metoden.
Ficks metod
Den föreslogs av Adolph Fick år 1870. Metoden bygger på antagandet att syretillförseln till lungorna i vila är lika med den mängd syre som används av vävnaderna, och mängden blod som stöts ut av vänsterkammaren är lika med volymen blod som flödar genom lungorna. Blandat venöst blod måste tas, eftersom syrekoncentrationen i blodet från vena cava och sinus coronarius skiljer sig avsevärt. Blod tas från högerkammaren eller lungartären, vilket är att föredra. Skillnaden i arteriovenöst syre kan bestämmas utifrån syrekoncentrationen i arteriellt (Ca) och venöst (Cv) blod. Genom att beräkna syrehalten som absorberas under 1 minut kan volymen blod som flödar genom lungorna under samma tidsperiod beräknas, dvs. hjärtminutvolymen (CO):
MO = Q / Ca - St (l/min),
Där Q är kroppens syreupptag (ml/min).
Med kännedom om hjärtindex kan man beräkna hjärtindex (KI). För att göra detta dividerar man hjärtindex med patientens gelyta, som beräknas utifrån patientens längd och kroppsvikt. Hjärtindex hos en vuxen är normalt 5–6 l/min, och KI är 2,8–3,5 l/min/ m2.
Termodilutionsmetod
Denna metod använder en kyld isoton natriumkloridlösning (5-10 ml), som förs in genom en multilumenkateter i höger förmak. Kateterns spets med termistorn är placerad i lungartären. Kalibrering av kurvorna utförs genom att kortvarigt slå på ett konstant motstånd, vilket ger avvikelser hos registreringsenheten motsvarande en viss temperaturförändring för en given termistor. De flesta termodilutionsenheter är utrustade med analoga datorer. Modern utrustning möjliggör upp till 3 mätningar av blodets MO inom 1 minut och flera upprepningar av studierna. Hjärtminutvolym, eller MO, bestäms med följande formel: MO = V (T1 - T2) x 60 x 1,08 / S (l/min),
Där V är volymen av den introducerade indikatorn; T1 är blodtemperaturen; T2 är indikatortemperaturen; S är arean under utspädningskurvan; 1,08 är koefficienten beroende på den specifika densiteten och värmekapaciteten hos blodet och den isotoniska natriumkloridlösningen.
Fördelarna med termodilution, liksom behovet av kateterisering av endast venbädden, gör denna metod för närvarande till den mest acceptabla för att bestämma hjärtminutvolymen i klinisk praxis.
Några tekniska aspekter av kateteriseringslaboratoriet
Personalen vid kateteriseringsangiografilaboratoriet omfattar chef, läkare, operationssjuksköterskor och röntgentekniker (röntgentekniker) om cine och storformatsröntgenfilmning används. I laboratorier som endast använder videofilmer och datoriserad bildinspelning behövs inte röntgentekniker. All laboratoriepersonal måste vara skicklig i hjärt-lungräddningstekniker, för vilka röntgenoperationssalen måste ha lämpliga läkemedel, en defibrillator, en apparat för elektrisk stimulering av hjärtat med en uppsättning elektrodkatetrar, en central syrgasförsörjning och (helst) en apparat för artificiell ventilation av lungorna.
Komplexa och riskabla diagnostiska ingrepp och PCI (angioplastik, stentning, aterektomi etc.) bör helst utföras på kliniker med ett hjärtkirurgiskt team. Enligt rekommendationerna från The American College of Cardiology/American Heart Association kan angioplastik och undersökning av patienter med hög risk för komplikationer, AMI, utföras av erfarna, kvalificerade specialister utan närvaro av hjärtkirurgiskt stöd på sjukhuset om patienten inte kan transporteras till en mer lämplig plats utan ytterligare risk. I Europa och vissa andra länder (inklusive Ryssland) utförs endovaskulära ingrepp i allt högre grad utan närvaro av hjärtkirurger, eftersom behovet av akut hjärtkirurgi för närvarande är extremt lågt. Ett avtal med en närliggande hjärtkirurgisk klinik är tillräckligt för akut överföring av patienten dit vid peri- och postoperativa komplikationer.
För att upprätthålla operatörernas lämplighet, kvalifikationer och skicklighet måste laboratoriet utföra minst 300 procedurer per år, och varje läkare måste utföra minst 150 diagnostiska procedurer per år. För kateterisering och angiografi krävs en högupplöst röntgenangiografienhet, ett system för övervakning av EKG och intravaskulärt tryck, arkivering och bearbetning av angiografiska bilder, sterila instrument och olika typer av katetrar (olika typer av katetrar för koronarangiografi beskrivs nedan). Angiografienheten måste vara utrustad med en anordning för kineangiografisk eller digital datorbildtagning och arkivering, ha möjlighet att hämta bilder online, dvs. omedelbart med kvantitativ datoranalys av angiogram.
Förändringar i intrakavitära tryckkurvor
Intrakavitära tryckkurvor kan förändras vid olika patologiska tillstånd. Dessa förändringar tjänar till diagnostik vid undersökning av patienter med olika hjärtsjukdomar.
För att förstå orsakerna till tryckförändringar i hjärtats hålrum är det nödvändigt att ha en uppfattning om de tidsmässiga sambanden mellan de mekaniska och elektriska processer som sker under hjärtcykeln. Amplituden för a-vågen i höger förmak är högre än amplituden för y-vågen. Ett överskott av y-vågen över a-vågen i tryckkurvan från höger förmak indikerar en störning av förmakets fyllnad under ventrikulär systole, vilket uppstår vid trikuspidalklaffens insufficiens eller en defekt.
Vid trikuspidalstenos liknar tryckkurvan i höger förmak den i vänster förmak vid mitralisstenos eller konstriktiv perikardit, med en minskning och platå i mellersta och sena diastolen, typiskt för förhöjt tryck under tidig systole. Det genomsnittliga vänster förmakstrycket motsvarar ganska nära pulmonalisartärens kiltryck och det pulmonalisstammdiastoliska trycket. Vid mitralisinsufficiens utan stenos sker en snabb tryckminskning vid systolens början (en minskning av y-vågen), följt av en gradvis ökning av sen diastole (diastas). Detta återspeglar uppnåendet av jämvikt mellan förmaks- och ventrikulärtryck under den sena fasen av ventrikulär fyllnad. Hos patienter med mitralisstenos minskar däremot y-vågen långsamt, medan trycket i vänster förmak fortsätter att minska under hela diastolen, och det finns inga tecken på diastas av pulstrycket i vänster förmak, eftersom den atrioventrikulära tryckgradienten bevaras. Om mitralisstenos åtföljs av en normal sinusrytm, bevaras α-vågen i vänster förmak och förmakens kontraktion orsakar skapandet av en stor tryckgradient. Hos patienter med isolerad mitralisregurgitation är v-vågen tydligt uttryckt och har en brant nedåtgående knäriktning av y-linjen.
På vänsterkammartryckkurvan föregår EDP-punkten omedelbart starten av dess isometriska kontraktion och är belägen omedelbart efter a-vågen före c-vågen för vänster förmakstryck. Vänsterkammar-EDP kan öka i följande fall: hjärtsvikt, om kammaren utsätts för en stor belastning orsakad av överdrivet blodflöde, till exempel vid aorta- eller mitralisinsufficiens; vänsterkammarhypertrofi, åtföljd av en minskning av dess töjbarhet, elasticitet och compliance; restriktiv kardiomyopati; konstriktiv perikardit; hjärttamponad orsakad av perikardiell effusion.
Vid aortastenos, som åtföljs av ett hindrat blodutflöde från vänster kammare och en ökning av trycket i den jämfört med det systoliska trycket i aorta, det vill säga uppkomsten av en tryckgradient, liknar vänsterkammartryckkurvan tryckkurvan under isometrisk kontraktion. Dess konturer är mer symmetriska, och det maximala trycket utvecklas senare än hos friska individer. En liknande bild observeras vid registrering av tryck i höger kammare hos patienter med pulmonell artärstenos. Blodtryckskurvor kan också skilja sig åt hos patienter med olika typer av aortastenos. Således observeras vid klaffstenos en långsam och fördröjd ökning av den arteriella pulsvågen, och vid hypertrofisk kardiomyopati ersätts den initiala kraftiga tryckökningen av en snabb minskning och sedan en sekundär positiv våg som återspeglar obstruktion under systole.
Härledda index för intraventrikulärt tryck
Förändrings-/ökningshastigheten för den intraventrikulära tryckkurvan under den isovolumiska kontraktionsfasen kallas den första derivatan - dр/dt. Tidigare användes den för att bedöma den ventrikulära myokardiets kontraktilitet. Värdet på dр/dt och den andra derivatan - dр/dt/р - beräknas från den intraventrikulära tryckkurvan med hjälp av elektronisk och datorteknik. De maximala värdena för dessa indikatorer representerar indexen för den ventrikulära kontraktionshastigheten och hjälper till att bedöma hjärtats kontraktilitet och inotropa status. Tyvärr tillåter det breda utbudet av dessa indikatorer i olika patientkategorier oss inte att utveckla några genomsnittliga standarder, men de är fullt tillämpliga på en patient med initialdata och mot bakgrund av användning av läkemedel som förbättrar hjärtmuskelns kontraktila funktion.
För närvarande, med tanke på att vi har i vår arsenal av patientundersökningsmetoder som ekokardiografi i dess olika modifieringar, datortomografi (CT), elektronstråle- och magnetisk resonanstomografi (MRI), är dessa indikatorer för att diagnostisera hjärtpatologier inte lika viktiga som tidigare.
Komplikationer av hjärtkateterisering
Hjärtkateterisering är relativt säkert, men liksom alla invasiva tekniker har den en viss andel komplikationer förknippade med både själva ingreppet och patientens allmänna tillstånd. Användningen av mer avancerade och tunna atraumatiska katetrar, lågosmolära och/eller nonjoniska RVS, moderna angiografiska enheter med datoriserad bildbehandling i realtid för invasiva ingrepp har avsevärt minskat incidensen av möjliga komplikationer. Således överstiger dödligheten under hjärtkateterisering i stora angiografiska laboratorier inte 0,1 %. S. Pepine et al. rapporterar en total dödlighet på upp till 0,14 %, med 1,75 % för patienter under 1 år, 0,25 % för personer över 60 år, 0,03 % för kranskärlssjukdom i ett kärl, 0,16 % för kranskärlssjukdom i tre kärl och 0,86 % för vänster kranskärlssjukdom. Vid hjärtsvikt ökar även dödligheten beroende på NUHA-klassen: vid I-II FC - 0,02 %, III och IV FC - 0,12 respektive 0,67 %. Hos vissa patienter är risken för allvarliga komplikationer ökad. Det handlar om patienter med instabil och progressiv angina, nyligen genomgången (mindre än 7 dagar) hjärtinfarkt, tecken på lungödem på grund av myokardischemi, med cirkulationssvikt i III-IV FC, svår högerkammarsvikt, hjärtklafffel (svår aortastenos och aortastens med ett pulstryck på mer än 80 mm Hg), medfödda hjärtfel med pulmonell hypertension och högerkammarsvikt.
I en multivariat analys av 58 332 patienter var prediktorer för allvarliga komplikationer svår hjärtsvikt, hypertoni, kranskärlssjukdom, aorta- och mitralisklaffsjukdom, njursvikt, instabil angina och akut hjärtinfarkt under de första 24 timmarna, samt kardiomyopati. Hos 80-åriga patienter ökade dödligheten under invasiva diagnostiska procedurer också till 0,8 %, och incidensen av vaskulära komplikationer vid punktionsstället nådde 5 %.


 [
[