Medicinsk expert av artikeln
Nya publikationer
Hjärtklaffar
Senast recenserade: 04.07.2025

Allt iLive-innehåll är mediekontrollerat eller faktiskt kontrollerat för att säkerställa så mycket faktuell noggrannhet som möjligt.
Vi har strikta sourcing riktlinjer och endast länk till välrenommerade media webbplatser, akademiska forskningsinstitut och, när det är möjligt, medicinsk peer granskad studier. Observera att siffrorna inom parentes ([1], [2] etc.) är klickbara länkar till dessa studier.
Om du anser att något av vårt innehåll är felaktigt, omodernt eller på annat sätt tveksamt, välj det och tryck på Ctrl + Enter.
Tidigare trodde man att alla hjärtklaffar var enkla strukturer vars bidrag till det enkelriktade blodflödet helt enkelt var passiv rörelse som svar på en applicerad tryckgradient. Denna förståelse av "passiva strukturer" ledde till utvecklingen av "passiva" mekaniska och biologiska klaffersättningar.
Det blir nu uppenbart att hjärtklaffar har en mer komplex struktur och funktion. Därför förutsätter skapandet av en "aktiv" hjärtklaffsersättning en betydande likhet i struktur och funktion med den naturliga hjärtklaffen, vilket i framtiden är ganska realistiskt tack vare utvecklingen av vävnadsteknik.
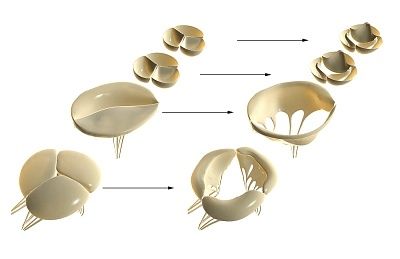
Hjärtklaffar utvecklas från embryonala rudiment av mesenkymal vävnad under bildandet av endokardiet. Under morfogenesen bildas atrioventrikulärkanalen (trikuspidal- och mitralisklaffar) och kammarens utflödeskanal (aorta- och pulmonella hjärtklaffar).
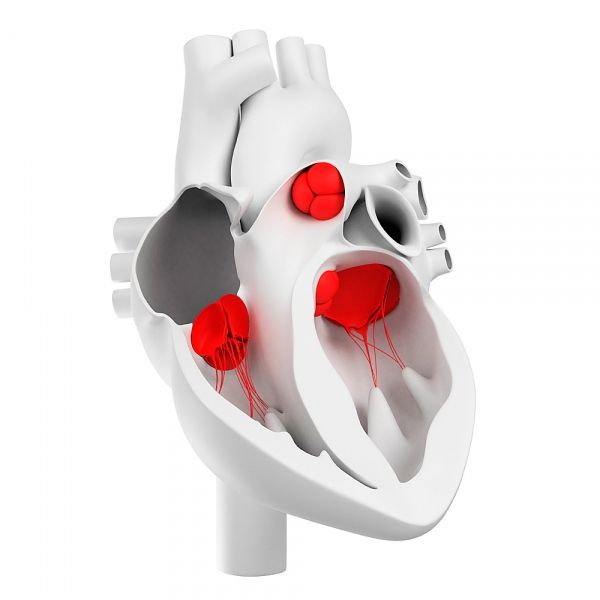
Hur är hjärtklaffarna arrangerade?
Studien av blodtillförseln till klaffarna initierades av N. Luschka (1852), som injicerade hjärtkärlen med en kontrastmassa. Han upptäckte ett flertal blodkärl i klaffarnas kuper i atrioventrikulära och semilunarklaffarna i aorta och lungartären. Samtidigt innehöll ett antal manualer om patologisk anatomi och histologi indikationer på att oförändrade mänskliga hjärtklaffar inte innehåller blodkärl, och de senare förekommer i klaffarna endast i olika patologiska processer - ateroskleros och endokardit av olika etiologier. Information om avsaknaden av blodkärl baserades huvudsakligen på histologiska studier. Det antogs att i avsaknad av blodkärl i den fria delen av kuperna sker deras näring genom att filtrera vätska från blodplasman som tvättar kuperna. Penetration av några kärl tillsammans med fibrer av tvärstrimmig muskelvävnad i klaffarnas och senackordorna noterades.
Vid injektion av hjärtkärl med olika färgämnen (bläck i gelatin, vismut i gelatin, vattenhaltig suspension av svart bläck, lösningar av karmin eller trypanblått) fann man emellertid att kärlen penetrerar atrioventrikulära hjärtklaffar, aortaklaffar och lungartär tillsammans med hjärtmuskelvävnaden, strax innan de når klaffens fria kant.
I den lösa fibrösa bindväven i atrioventrikulära klaffkuspar hittades enskilda huvudkärl som anastomoserade med kärl i angränsande områden av tvärstrimmig hjärtmuskelvävnad.
Det största antalet blodkärl var belägna vid basen och ett jämförelsevis mindre antal i den fria delen av dessa klaffar.
Enligt KI Kulchitsky et al. (1990) finns en större diameter på arteriella och venösa kärl i mitralisklaffen. Vid basen av denna klaffs kupor finns huvudsakligen huvudkärlen med ett smalt slingnätverk av kapillärer, som penetrerar den basala delen av kupen och upptar 10% av dess area. I trikuspidalklaffen har arteriella kärl en mindre diameter än i mitralisklaffen. I denna klaffs kupor finns huvudsakligen spridda kärl och jämförelsevis breda slingor av blodkapillärer. I mitralisklaffen försörjs den främre kupen med blod mer intensivt, i trikuspidalklaffen - de främre och bakre kuporna, som utför den huvudsakliga stängningsfunktionen. Förhållandet mellan diametrarna för de arteriella och venösa kärlen i atrioventrikulärklaffarna i hjärtat hos mogna personer är 1:1,5. Kapillärslingorna är polygonala och är belägna vinkelrätt mot basen av klaffkuporna. Kärlen bildar ett plant nätverk beläget under endotelet på förmakssidan. Blodkärl finns också i tendinsträngarna, där de penetrerar från papillarmusklerna i höger och vänster kammare på ett avstånd av upp till 30 % av tendinsträngarnas längd. Många blodkärl bildar bågformade öglor vid basen av tendinsträngarna. Hjärtklaffarna i aorta och pulmonalisstammen skiljer sig avsevärt från atrioventrikulärklaffarna vad gäller blodförsörjning. Huvudkärlen med relativt mindre diameter närmar sig basen av aorta- och pulmonalisklaffarnas halvmånade kuspar. De korta grenarna av dessa kärl slutar i kapillärsträngar med oregelbunden oval och polygonal form. De är huvudsakligen belägna nära basen av halvmånade kuspar. De venösa kärlen vid basen av aorta- och pulmonalisklaffarna har också en mindre diameter än de vid basen av atrioventrikulärklaffarna. Förhållandet mellan diametrarna för de arteriella och venösa kärlen i aorta- och pulmonalisklaffarna i hjärtat hos mogna personer är 1:1,4. Korta laterala grenar sträcker sig från de större kärlen och slutar i kapillärsträngar med oregelbunden oval och polygonal form.

Med åldern sker en förgrovning av bindvävsfibrer, både kollagena och elastiska, samt en minskning av mängden lös fibrös oformad bindväv, skleros i vävnaden i atrioventrikulärklaffarna och halvmånsklaffarna i aorta- och pulmonalartärklaffarna utvecklas. Längden på de tvärstrimmiga hjärtfibrerna i klaffarna minskar, och följaktligen minskar deras mängd och antalet blodkärl som penetrerar hjärtklaffarna. På grund av dessa förändringar förlorar hjärtklaffarna sina elastiska och fjädrande egenskaper, vilket påverkar mekanismen för klaffstängning och hemodynamik.
Hjärtklaffarna har nätverk av lymfkapillärer och ett litet antal lymfkärl utrustade med klaffar. De lymfatiska kapillärerna i klaffarnas lumen har ett karakteristiskt utseende: deras lumen är mycket ojämn, samma kapillär har olika diameter på olika ställen. På platser där flera kapillärer går samman bildas utvidgningar - lacunaer av olika former. Nätverkens öglor är ofta oregelbundna polygonala, mer sällan ovala eller runda. Ofta är de lymfatiska nätverkens öglor inte stängda, och de lymfatiska kapillärerna slutar blint. De lymfatiska kapillärernas öglor är oftast orienterade i riktning från klaffens fria kant till dess bas. I vissa fall har ett tvåskiktat nätverk av lymfatiska kapillärer hittats i atrioventrikulärklaffens klaffar.
De endokardiella nervplexuserna är belägna i sina olika lager, huvudsakligen under endotelet. Vid den fria kanten av klaffspetsarna är nervfibrerna huvudsakligen radiellt belägna och anslutna till de sena kordorna. Närmare basen av spetsarna bildas en stormaskig nervplexus, som ansluter till plexusen som är belägen runt de fibrösa ringarna. På de halvmånade spetsarna är det endokardiella nervnätet glesare. Vid klaffarnas fäste blir det tätt och flerskiktat.
Cellstrukturen hos hjärtklaffarna
Klaffinterstitiella celler, som ansvarar för att upprätthålla klaffens struktur, har en långsträckt form med många fina utskott som sträcker sig genom hela klaffmatrisen. Det finns två populationer av klaffinterstitiella celler som skiljer sig åt i morfologi och struktur; den ena har kontraktila egenskaper och kännetecknas av närvaron av kontraktila fibriller, den andra har sekretoriska egenskaper och har ett välutvecklat endoplasmatiskt retikulum och Golgi-apparat. Den kontraktila funktionen motstår hemodynamiskt tryck och stöds vidare av produktionen av både hjärt- och skelettkontraktila proteiner, vilka inkluderar de tunga kedjorna av alfa- och beta-myosin och olika isoformer av troponin. Kontraktion av hjärtklaffens klaffblad har visats som svar på ett antal vasoaktiva medel, vilket tyder på en koordinerad biologisk stimulans för framgångsrik klafffunktion.
Interstitiella celler är också viktiga komponenter i reparationssystemet hos strukturer som hjärtklaffar. Den konstanta rörelsen av klaffbladen och den därmed sammanhängande bindvävsdeformationen orsakar skador som de interstitiella klaffcellerna reagerar på för att bibehålla klaffens integritet. Reparationsprocessen verkar vara avgörande för normal klafffunktion, och frånvaron av dessa celler i nuvarande modeller av artificiella klaffar är sannolikt en bidragande faktor till de strukturella skadorna på bioproteser.
Ett viktigt forskningsområde inom interstitiella celler är studiet av interaktioner mellan dem och den omgivande matrisen medierade av fokala adhesionsmolekyler. Fokala adhesioner är specialiserade cell-matrix-interaktionsställen som länkar cellcytoskelettet till matrixproteiner via integriner. De fungerar också som signaltransduktionsställen och vidarebefordrar mekanisk information från den extracellulära matrisen som kan framkalla reaktioner inklusive, men inte begränsat till, celladhesion, migration, tillväxt och differentiering. Att förstå cellbiologin hos interstitiella klaffceller är avgörande för att belysa de mekanismer genom vilka dessa celler interagerar med varandra och sin omgivning, så att denna funktion kan återges i artificiella klaffar.
I samband med utvecklingen av en lovande inriktning inom vävnadsteknik för hjärtklaffar utförs studier av interstitiella celler med hjälp av ett brett spektrum av tekniker. Närvaron av cellcytoskelettet bekräftas genom färgning för vimentin, desmin, troponin, alfa-aktin och glattmuskelmyosin, tunga kedjor av alfa- och beta-myosin, lätta kedjor-2 av hjärtmyosin, alfa- och beta-tubulin. Cellkontraktilitet bekräftas genom ett positivt svar på adrenalin, angiotensin II, bradykinin, karbakol, kaliumklorid, endotel I. Cellulära relationer bestäms genom funktionella gapinteraktioner och verifieras genom mikroinjektioner av karboxifluorescein. Matrissekretion etableras genom färgning för prolyl-4-hydroxylas/kollagen typ II, fibronektin, kondroitinsulfat, laminin. Innervation etableras genom den nära placeringen av motoriska nervändar, vilket återspeglas av aktiviteten hos neuropeptid Y tyrosinhydroxylas, acetylkolinesteras, vasoaktiv intestinal polypeptid, substans-P, capsicumgenrelaterad peptid. Mitogena faktorer uppskattas med hjälp av trombocytderiverad tillväxtfaktor, basisk fibroblasttillväxtfaktor, serotonin (5-HT). De studerade interstitiella cellfibroblasterna kännetecknas av ett ofullständigt basalmembran, långa, tunna cytoplasmatiska processer, nära förbindelse med matrisen, välutvecklat ojämnt endoplasmatiskt retikulum och Golgi-apparat, rikedom av mikrofilament och bildning av adhesiva bindningar.
Klaffceller i endokardiet bildar en funktionell atrombogen mantel runt varje hjärtklaff, liknande det vaskulära endotelet. Den allmänt använda metoden för klaffbyte eliminerar endokardiets skyddande funktion, vilket kan leda till trombocyt- och fibrinavsättning på artificiella klaffar, utveckling av bakteriell infektion och vävnadsförkalkning. En annan sannolik funktion hos dessa celler är regleringen av de underliggande interstitiella klaffcellerna, liknande regleringen av glatta muskelceller av endotelet. Komplexa interaktioner existerar mellan endotelet och angränsande celler, delvis medierade av lösliga faktorer som utsöndras av endotelcellerna. Dessa celler bildar en enorm yta täckt med mikroutsprång på den luminala sidan, vilket ökar exponeringen och möjlig interaktion med metaboliska substanser i det cirkulerande blodet.
Endotelet uppvisar ofta morfologiska och funktionella skillnader orsakade av skjuvspänningar på kärlväggen på grund av blodflöde, och detta gäller även de klaffendokardiella cellerna, som antar antingen en avlång eller polygonal form. Förändringar i cellstrukturen kan uppstå på grund av lokal hemodynamiks inverkan på komponenter i cellens cytoskelett eller sekundära effekter orsakade av förändringar i den underliggande extracellulära matrisen. På ultrastrukturell nivå har klaffendokardiella celler intercellulära förbindelser, plasmavesiklar, ett grovt endoplasmatiskt retikulum och en Golgi-apparat. Även om de producerar von Willebrand-faktor både in vivo och in vitro, saknar de Weibel-Palade-kroppar (specifika granuler som innehåller von Willebrand-faktor), vilka är organeller som är karakteristiska för det vaskulära endotelet. Klaffendokardiella celler kännetecknas av starka förbindelser, funktionella gapinteraktioner och överlappande marginalveck.
Endokardiella celler behåller sin metaboliska aktivitet även in vitro: de producerar von Willebrands faktor, prostacyklin, kväveoxidsyntas, uppvisar aktivitet som angiotensinkonverterande enzym och utsöndrar intensivt adhesionsmolekylerna ICAM-1 och ELAM-1, vilka är viktiga för att binda mononukleära celler under utvecklingen av ett immunsvar. Alla dessa markörer bör beaktas vid odling av en ideal cellkultur för att skapa en artificiell klaff med hjälp av vävnadsteknik, men den immunstimulerande potentialen hos själva klaffendokardiella celler kan begränsa deras användning.
Hjärtklaffarnas extracellulära matris består av fibröst kollagen och elastin, makromolekyler, proteoglykaner och glykoproteiner. Kollagen står för 60 % av klaffens torrvikt, elastin för 10 % och proteoglykaner för 20 %. Kollagenkomponenten ger klaffens huvudsakliga mekaniska stabilitet och representeras av kollagener av typ I (74 %), II (24 %) och V (2 %). Buntar av kollagentrådar är omgivna av en elastinmantel, som medierar interaktioner mellan dem. Glykosaminoglykansidkedjorna i proteoglykanmolekyler tenderar att bilda en geliknande substans i vilken andra matrismolekyler interagerar för att bilda permanenta bindningar och andra komponenter deponeras. Glykosaminoglykaner i mänskliga hjärtklaffar består huvudsakligen av hyaluronsyra, i mindre utsträckning av dermatansulfat, kondroitin-4-sulfat och kondroitin-6-sulfat, med en minimal mängd heparansulfat. Ombyggnad och förnyelse av matrixvävnad regleras av matrixmetalloproteinaser (MMP) och deras vävnadshämmare (TI). Dessa molekyler är också involverade i ett bredare spektrum av fysiologiska och patologiska processer. Vissa metalloproteinaser, inklusive interstitiella kollagenaser (MMP-1, MMP-13) och gelatinaser (MMP-2, MMP-9) och deras vävnadshämmare (TI-1, TI-2, TI-3), finns i alla hjärtklaffar. Överproduktion av metalloproteinaser är karakteristiskt för patologiska tillstånd i hjärtklaffen.
 [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ]
[ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ]
Hjärtklaffar och deras morfologiska struktur
Hjärtklaffar består av tre morfologiskt olika och funktionellt signifikanta lager av klaffmatrisen: fibrösa, svampiga och ventrikulära.
Det fibrösa lagret bildar ett belastningsbeständigt ramverk för klaffbladet, bestående av lager av kollagenfibrer. Dessa fibrer är radiellt anordnade i veck för att låta arteriklaffarna sträckas ut vid stängning. Det fibrösa lagret ligger nära utloppsytan på dessa klaffar. Det fibrösa lagret i atrioventrikulärklaffarna fungerar som en fortsättning på kollagenbuntarna i chordae tendineae. Det är beläget mellan det svampiga (inlopps-) och ventrikulära (utlopps-) lagret.
Mellan fibrösa och ventrikulära skikt finns det svampiga lagret (spongiosa). Det svampiga lagret består av dåligt organiserad bindväv i ett visköst medium. De dominerande matrixkomponenterna i detta lager är proteoglykaner med slumpmässigt orienterat kollagen och tunna lager av elastin. Sidokedjorna i proteoglykanmolekylerna bär en stark negativ laddning, vilket påverkar deras höga förmåga att binda vatten och bilda en porös matrixgel. Matrisens svampiga lager minskar mekanisk stress i hjärtklaffarnas klaffblad och bibehåller deras flexibilitet.
Ventrikulärskiktet är mycket tunnare än de andra och är rikt på elastiska fibrer som gör att vävnaden kan motstå konstant deformation. Elastin har en svampig struktur som omger och förbinder kollagenfibrer och håller dem i ett neutralt veckat tillstånd. Klaffens inloppsskikt (ventrikulärt - för arteriella klaffar och svampigt - för atrioventrikulärt) innehåller mer elastin än utloppet, vilket mjukar upp den hydrauliska chocken när kusparna stängs. Detta förhållande mellan kollagen och elastin gör att kusparna kan töjas upp till 40 % utan stabil deformation. När de utsätts för en liten belastning är kollagenstrukturerna i detta skikt orienterade i belastningens riktning, och dess motståndskraft mot ytterligare belastningstillväxt ökar.
Således är idén om hjärtklaffarna som enkla endokardiella dubbletter inte bara förenklad utan också i grunden felaktig. Hjärtklaffar är komplexa organ som inkluderar tvärstrimmiga muskelfibrer, blod- och lymfkärl samt nervelement. Både i sin struktur och i sin funktion är klaffarna integrerade i alla hjärtstrukturer. Analys av normal klafffunktion måste ta hänsyn till dess cellulära organisation, såväl som cellernas interaktion med varandra och matrisen. Kunskapen som erhållits från sådana studier är ledande inom design och utveckling av klaffproteser med hjälp av vävnadsteknik.

