Medicinsk expert av artikeln
Nya publikationer
Diagnos av osteoartrit: magnetisk resonanstomografi
Senast recenserade: 04.07.2025

Allt iLive-innehåll är mediekontrollerat eller faktiskt kontrollerat för att säkerställa så mycket faktuell noggrannhet som möjligt.
Vi har strikta sourcing riktlinjer och endast länk till välrenommerade media webbplatser, akademiska forskningsinstitut och, när det är möjligt, medicinsk peer granskad studier. Observera att siffrorna inom parentes ([1], [2] etc.) är klickbara länkar till dessa studier.
Om du anser att något av vårt innehåll är felaktigt, omodernt eller på annat sätt tveksamt, välj det och tryck på Ctrl + Enter.
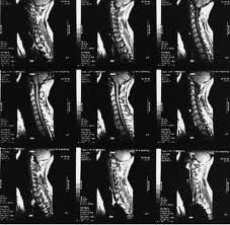
Magnetisk resonanstomografi (MRT) har blivit en av de ledande metoderna för icke-invasiv diagnostik av artros under senare år. Sedan 1970-talet, då principerna för magnetisk resonans (MR) först användes för att studera människokroppen, har denna metod för medicinsk avbildning förändrats dramatiskt och fortsätter att utvecklas snabbt.
Teknisk utrustning och programvara förbättras, bildinsamlingsmetoder utvecklas och kontrastmedel för MR-undersökningar utvecklas. Detta gör det möjligt att ständigt hitta nya tillämpningsområden för MR. Om dess tillämpning först var begränsad till studier av det centrala nervsystemet, används MR nu framgångsrikt inom nästan alla områden inom medicin.
År 1946 upptäckte grupper av forskare från Stanford- och Harvarduniversiteten oberoende av varandra ett fenomen som kallas kärnmagnetisk resonans (NMR). Dess kärna var att kärnorna i vissa atomer, som befinner sig i ett magnetfält, under påverkan av ett externt elektromagnetiskt fält, kan absorbera energi och sedan avge den i form av en radiosignal. För denna upptäckt tilldelades F. Bloch och E. Parmel Nobelpriset 1952. Det nya fenomenet användes snart för spektralanalys av biologiska strukturer (NMR-spektroskopi). År 1973 demonstrerade Paul Rautenburg för första gången möjligheten att erhålla en bild med hjälp av NMR-signaler. Så uppstod NMR-tomografi. De första NMR-tomogrammen av en levande människas inre organ demonstrerades 1982 vid den internationella radiologkongressen i Paris.
Två förtydliganden bör ges. Trots att metoden är baserad på NMR-fenomenet kallas den magnetisk resonans (MR), varvid ordet "kärnkraft" utelämnas. Detta görs så att patienter inte ska tänka på radioaktivitet i samband med atomkärnans sönderfall. Och den andra omständigheten: MR-tomografer är inte av misstag "inställda" på protoner, dvs. vätekärnor. Det finns mycket av detta element i vävnader, och dess kärnor har det största magnetiska momentet bland alla atomkärnor, vilket avgör en ganska hög nivå av MR-signal.
Om det år 1983 bara fanns ett fåtal apparater lämpliga för klinisk forskning i världen, så fanns det i början av 1996 cirka 10 000 tomografer i drift världen över. Varje år introduceras 1000 nya apparater i praktiken. Mer än 90 % av parken av MR-tomografer är modeller med supraledande magneter (0,5–1,5 T). Det är intressant att notera att om företagen – tillverkare av MR-tomografer – i mitten av 80-talet vägleddes av principen "ju högre fält, desto bättre", med fokus på modeller med ett fält på 1,5 T och högre, så blev det i slutet av 80-talet tydligt att de inom de flesta tillämpningsområden inte har några betydande fördelar jämfört med modeller med en genomsnittlig fältstyrka. Därför ägnar de största tillverkarna av MR-tomografer (General Electric, Siemens, Philips, Toshiba, Picker, Bruker, etc.) för närvarande stor uppmärksamhet åt produktion av modeller med medelhöga och till och med låga fält, vilka skiljer sig från högfältssystem genom sin kompakthet och ekonomi med tillfredsställande bildkvalitet och betydligt lägre kostnad. Högfältssystem används främst i forskningscentra för MR-spektroskopi.
Principen för MR-metoden
Huvudkomponenterna i en MR-skanner är: en superstark magnet, en radiosändare, en mottagande radiofrekvensspole, en dator och en kontrollpanel. De flesta enheter har ett magnetfält med ett magnetiskt moment parallellt med människokroppens längdaxel. Magnetfältets styrka mäts i tesla (T). För klinisk MR används fält med en styrka på 0,2–1,5 T.
När en patient placeras i ett starkt magnetfält vrider sig alla protoner, som är magnetiska dipoler, i det yttre fältets riktning (som en kompassnål orienterad mot jordens magnetfält). Dessutom börjar varje protons magnetiska axlar att rotera runt det yttre magnetfältets riktning. Denna specifika rotationsrörelse kallas procession, och dess frekvens kallas resonansfrekvens. När korta elektromagnetiska radiofrekvenspulser passerar genom patientens kropp, orsakar radiovågornas magnetfält att alla protoners magnetiska moment roterar runt det yttre fältets magnetiska moment. För att detta ska ske måste radiovågornas frekvens vara lika med protonernas resonansfrekvens. Detta fenomen kallas magnetisk resonans. För att ändra de magnetiska protonernas orientering måste protonernas och radiovågornas magnetfält resonera, dvs. ha samma frekvens.
Ett nettomagnetiskt moment skapas i patientens vävnader: vävnaderna magnetiseras och deras magnetism är orienterad strikt parallellt med det externa magnetfältet. Magnetismen är proportionell mot antalet protoner per volymenhet vävnad. Det enorma antalet protoner (vätekärnor) som finns i de flesta vävnader innebär att det nettomagnetiska momentet är tillräckligt stort för att inducera en elektrisk ström i en mottagarspole som är placerad utanför patienten. Dessa inducerade MR-signaler används för att rekonstruera MR-bilden.
Processen där elektronerna i kärnan går från exciterat tillstånd till jämviktstillstånd kallas spin-gitterrelaxationsprocessen eller longitudinell relaxation. Den kännetecknas av T1 - spin-gitterrelaxationstiden - den tid som krävs för att överföra 63 % av kärnorna till jämviktstillstånd efter excitation med en 90°-puls. T2 - spin-spinnrelaxationstiden utmärks också.
Det finns flera metoder för att erhålla MR-tomogram. De skiljer sig åt i ordningen och typen av generering av radiofrekvenspulser och metoder för MR-signalanalys. De två mest använda metoderna är spin-lattice och spin-eko. Spin-lattice analyserar huvudsakligen T1-relaxationstiden. Olika vävnader (grå och vit substans i hjärnan, cerebrospinalvätska, tumörvävnad, brosk, muskler etc.) innehåller protoner med olika T1-relaxationstider. MR-signalens intensitet är relaterad till T1:s varaktighet: ju kortare T1, desto intensivare är MR-signalen och desto ljusare visas det givna området av bilden på TV-skärmen. Fettvävnad är vit på MR-tomogram, följt av hjärnan och ryggmärgen, täta inre organ, kärlväggar och muskler i fallande ordning efter MR-signalintensitet. Luft, ben och förkalkningar producerar praktiskt taget ingen MR-signal och visas därför i svart. Dessa T1-relationer mellan relaxationstider skapar förutsättningarna för att visualisera normala och förändrade vävnader på MR-skanningar.
I en annan MR-metod, kallad spin-eko, riktas en serie radiofrekvenspulser mot patienten, vilket roterar de precesserande protonerna 90°. Efter att pulserna upphört registreras MR-responssignalerna. Emellertid är responssignalens intensitet relaterad till T2-tiden: ju kortare T2, desto svagare signal och följaktligen desto lägre ljusstyrka på glödet på TV-skärmen. Således är den slutliga MR-bilden med T2-metoden motsatsen till den med T1-metoden (eftersom ett negativt är motsatsen till ett positivt).
MR-tomografi visar mjukvävnader bättre än datortomografi: muskler, fettlager, brosk och blodkärl. Vissa apparater kan producera bilder av blodkärl utan att injicera kontrastmedel (MR-angiografi). På grund av den låga vattenhalten i benvävnad skapar den senare inte en avskärmande effekt, som vid röntgen-CT-skanning, dvs. den stör inte bilden av till exempel ryggmärgen, mellankotsdiskarna etc. Naturligtvis finns vätekärnor inte bara i vatten, utan i benvävnaden är de fixerade i mycket stora molekyler och täta strukturer och stör inte MR.
Fördelar och nackdelar med MR
De främsta fördelarna med MR inkluderar icke-invasivitet, ofarlighet (ingen strålningsexponering), tredimensionell bildtagning, naturlig kontrast från rörligt blod, inga artefakter från benvävnad, hög differentiering av mjukvävnader, möjligheten att utföra MP-spektroskopi för in vivo-studier av vävnadsmetabolism. MR möjliggör erhållande av bilder av tunna lager av människokroppen i vilken sektion som helst - i frontala, sagittala, axiella och sneda plan. Det är möjligt att rekonstruera volymetriska bilder av organ, synkronisera bildtagningen av tomogram med elektrokardiogrammets tänder.
De största nackdelarna inkluderar vanligtvis den relativt långa tiden det tar att ta bilder (vanligtvis minuter), vilket leder till att artefakter uppstår från andningsrörelser (detta minskar särskilt effektiviteten av lungundersökning), arytmier (vid hjärtundersökning), oförmågan att tillförlitligt detektera stenar, förkalkningar, vissa typer av benpatologi, höga kostnader för utrustning och dess drift, speciella krav på de lokaler där apparaterna är placerade (avskärmning från störningar), oförmågan att undersöka patienter med klaustrofobi, artificiella pacemakers, stora metallimplantat gjorda av icke-medicinska metaller.
 [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
[ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
Kontrastmedel för MR
I början av användningen av MR trodde man att den naturliga kontrasten mellan olika vävnader eliminerade behovet av kontrastmedel. Man upptäckte snart att skillnaden i signaler mellan olika vävnader, dvs. kontrasten i MR-bilden, kunde förbättras avsevärt med kontrastmedel. När det första MR-kontrastmedlet (innehållande paramagnetiska gadoliniumjoner) blev kommersiellt tillgängligt ökade det diagnostiska informationsinnehållet i MR avsevärt. Kärnan i att använda MR-kontrastmedel är att ändra de magnetiska parametrarna för vävnads- och organprotoner, dvs. att ändra relaxationstiden (TR) för T1- och T2-protoner. Idag finns det flera klassificeringar av MR-kontrastmedel (eller snarare kontrastmedel - CA).
Enligt den dominerande effekten på relaxationstiden delas MR-KA in i:
- T1-CA, som förkortar T1 och därigenom ökar intensiteten hos vävnadens MP-signal. De kallas även positiv CA.
- T2-CA som förkortar T2, vilket minskar intensiteten hos MR-signalen. Dessa är negativa CA.
Beroende på deras magnetiska egenskaper är MR-CA indelade i paramagnetiska och superparamagnetiska:
 [ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ]
[ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ]
Paramagnetiska kontrastmedel
Paramagnetiska egenskaper innehas av atomer med en eller flera oparade elektroner. Dessa är magnetiska joner av gadolinium (Gd), krom, nickel, järn och mangan. Gadoliniumföreningar har fått den bredaste kliniska tillämpningen. Gadoliniums kontrasteffekt beror på förkortningen av relaxationstiden T1 och T2. I låga doser dominerar effekten på T1, vilket ökar signalintensiteten. I höga doser dominerar effekten på T2, vilket minskar signalintensiteten. Paramagneter används nu mest inom klinisk diagnostisk praxis.
Superparamagnetiska kontrastmedel
Den dominerande effekten av superparamagnetisk järnoxid är en förkortning av T2-relaxationen. Med ökande dos minskar signalintensiteten. Ferromagnetiska CA:er, vilka inkluderar ferromagnetiska järnoxider som strukturellt liknar magnetitferrit (Fe2 +OFe23+ O3 ), kan också inkluderas i denna grupp av CA:er.
Följande klassificering är baserad på farmakokinetiken för CA (Sergeev PV et al., 1995):
- extracellulär (vävnadsospecifik);
- mag-tarmkanalen;
- organotropisk (vävnadsspecifik);
- makromolekylära, som används för att bestämma det vaskulära utrymmet.
I Ukraina är fyra MR-CA kända, vilka är extracellulära vattenlösliga paramagnetiska CA, av vilka gadodiamid och gadopentetinsyra används i stor utsträckning. De återstående grupperna av CA (2-4) genomgår kliniska prövningar utomlands.
Extracellulär vattenlöslig MR-CA
Internationellt namn |
Kemisk formel |
Strukturera |
Gadopentetisk syra |
Gadoliniumdimeglumindietylentriaminpentaacetat ((NMG)2Gd-DTPA) |
Linjär, jonisk |
Gadotersyra |
(NMG)Gd-DOTA |
Cyklisk, jonisk |
Gadodiamid |
Gadoliniumdietylentriaminpentaacetat-bis-metylamid (Gd-DTPA-BMA) |
Linjär, icke-jonisk |
Gadoteridol |
Gd-HP-D03A |
Cyklisk, nonjonisk |
Extracellulära CA administreras intravenöst, 98% av dem utsöndras via njurarna, penetrerar inte blod-hjärnbarriären, har låg toxicitet och tillhör gruppen paramagnetiska ämnen.
Kontraindikationer för MR
Absoluta kontraindikationer inkluderar tillstånd där undersökningen utgör ett hot mot patienternas liv. Till exempel förekomsten av implantat som aktiveras elektroniskt, magnetiskt eller mekaniskt - dessa är främst artificiella pacemakers. Exponering för radiofrekvent strålning från en MR-skanner kan störa funktionen hos en pacemaker som arbetar i njursystemet, eftersom förändringar i magnetfält kan imitera hjärtaktivitet. Magnetisk attraktion kan också få pacemakern att förskjutas i sin sockel och flytta elektroderna. Dessutom skapar magnetfältet hinder för funktionen av ferromagnetiska eller elektroniska mellanöreimplantat. Förekomsten av artificiella hjärtklaffar är farlig och är en absolut kontraindikation endast vid undersökning på MR-skannrar med höga fält, och om skador på klaffen misstänks kliniskt. Absoluta kontraindikationer för undersökningen inkluderar också förekomsten av små kirurgiska metallimplantat (hemostatiska klämmor) i centrala nervsystemet, eftersom deras förskjutning på grund av magnetisk attraktion hotar blödning. Deras närvaro i andra delar av kroppen utgör ett mindre hot, eftersom fibros och inkapsling av klämmorna efter behandling hjälper till att hålla dem stabila. Utöver den potentiella faran orsakar dock närvaron av metalliska implantat med magnetiska egenskaper artefakter som skapar svårigheter att tolka studiens resultat.
Kontraindikationer för MR
Absolut: |
Relativ: |
Pacemakers |
Andra stimulantia (insulinpumpar, nervstimulatorer) |
Ferromagnetiska eller elektroniska mellanöreimplantat |
Icke-ferromagnetiska innerörsimplantat, hjärtklaffsproteser (i höga fält, om dysfunktion misstänks) |
Hemostatiska klämmor av hjärnkärl |
Hemostatiska klämmor på andra ställen, dekompenserad hjärtsvikt, graviditet, klaustrofobi, behov av fysiologisk övervakning |
Relativa kontraindikationer, utöver de som anges ovan, inkluderar dekompenserad hjärtsvikt, behovet av fysiologisk övervakning (mekanisk ventilation, elektriska infusionspumpar). Klaustrofobi är ett hinder för studien i 1-4% av fallen. Det kan övervinnas, å ena sidan, genom att använda apparater med öppna magneter, å andra sidan - genom en detaljerad förklaring av apparaten och undersökningens förlopp. Det finns inga bevis för en skadlig effekt av MR på embryot eller fostret, men det rekommenderas att undvika MR under graviditetens första trimester. Användning av MR under graviditet är indicerat i fall där andra icke-joniserande diagnostiska avbildningsmetoder inte ger tillfredsställande information. MR-undersökning kräver mer patientmedverkan än datortomografi, eftersom patientens rörelser under undersökningen har en mycket större effekt på bildernas kvalitet, så undersökning av patienter med akut patologi, nedsatt medvetande, spastiska tillstånd, demens, såväl som barn är ofta svår.

