Medicinsk expert av artikeln
Nya publikationer
Bisköldkörtlarna
Senast recenserade: 04.07.2025

Allt iLive-innehåll är mediekontrollerat eller faktiskt kontrollerat för att säkerställa så mycket faktuell noggrannhet som möjligt.
Vi har strikta sourcing riktlinjer och endast länk till välrenommerade media webbplatser, akademiska forskningsinstitut och, när det är möjligt, medicinsk peer granskad studier. Observera att siffrorna inom parentes ([1], [2] etc.) är klickbara länkar till dessa studier.
Om du anser att något av vårt innehåll är felaktigt, omodernt eller på annat sätt tveksamt, välj det och tryck på Ctrl + Enter.
År 1879 beskrev den svenske forskaren S. Sandström bisköldkörtlarna hos människor och gav dem ett namn. Bisköldkörtlarna är vitala organ. Deras funktion är att producera och utsöndra bisköldkörtelhormon (PTH), en av de viktigaste regulatorerna av kalcium- och fosformetabolism.
Den parade övre bisköldkörteln (glandula parathyroidea superior) och den nedre bisköldkörteln (glandula parathyroidea inferior) är runda eller äggformade kroppar belägna på baksidan av var och en av sköldkörtelns lober: en körtel överst, den andra underst. Längden på varje körtel är 4-8 mm, bredden är 3-4 mm, tjockleken är 2-3 mm. Antalet av dessa körtlar är inte konstant och kan variera från 2 till 7-8, i genomsnitt är det fyra. Körtlarnas totala massa är i genomsnitt 1,18 g.
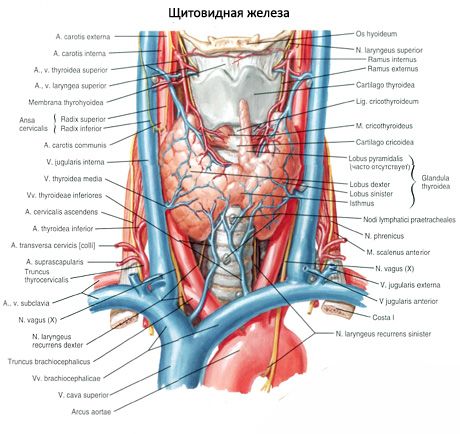
Bisköldkörtlarna skiljer sig från sköldkörteln genom sin ljusare färg (hos barn är de ljusrosa, hos vuxna - gulbruna). Ofta är bisköldkörtlarna belägna där sköldkörtelvävnaden penetreras av de nedre sköldkörtelartärerna eller deras grenar. Bisköldkörtlarna är separerade från de omgivande vävnaderna av en egen fibrös kapsel, från vilken bindvävsskikt sträcker sig in i körtlarna. De senare innehåller ett stort antal blodkärl och delar upp bisköldkörtlarna i grupper av epitelceller.
Körtlarnas parenkym bildas av huvud- och acidofila paratyrocyter, vilka bildar strängar och kluster omgivna av tunna buntar av bindvävsfibrer. Båda typerna av celler betraktas som olika stadier av paratyrocyternas utveckling. Huvudparatyrocyterna har en polyedrisk form, basofil cytoplasma med ett stort antal ribosomer. Bland dessa celler skiljer sig mörka (aktivt utsöndrande) och ljusa (mindre aktiva). Acidofila paratyrocyter är stora, med tydliga konturer, innehåller många små mitokondrier med glykogenpartiklar.
Bisköldkörtelhormonet paratyroxin (paratyroidhormon) har en proteinliknande sammansättning och är involverat i regleringen av fosfor-kalciummetabolismen. Paratyroidhormon minskar kalciumutsöndringen i urinen och ökar dess absorption i tarmen i närvaro av vitamin D. Tyrokalcitonin är en antagonist till paratyroidhormon.
Embryogenes av bisköldkörtlarna
Bisköldkörtlarna utvecklas från epitelet i de parade III och IV gälfickorna. Under den sjunde utvecklingsveckan separerar kroppens epitelrubriker från gälfickornas väggar och rör sig under tillväxtprocessen i kaudal riktning. Därefter intar de bildande bisköldkörtlarna en permanent position för dem på de bakre ytorna av sköldkörtelns högra och vänstra lober.
 [ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ]
[ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ]
Kärl och nerver i bisköldkörtlarna
Blodförsörjningen till bisköldkörtlarna tillhandahålls av grenar av de övre och nedre sköldkörtelartärerna, såväl som grenarna av esofagus och trakeal. Venöst blod flyter ut genom venerna med samma namn. Bisköldkörtelns innervation liknar sköldkörtelns innervation.
Åldersrelaterade egenskaper hos bisköldkörtlarna
Den totala massan av bisköldkörtlarna hos en nyfödd varierar mellan 6 och 9 mg. Under det första levnadsåret ökar deras totala massa 3-4 gånger, vid 5 års ålder fördubblas den igen och vid 10 års ålder tredubblas den. Efter 20 år når den totala massan av de fyra bisköldkörtlarna 120-140 mg och förblir konstant fram till hög ålder. I alla åldrar är massan av bisköldkörtlarna hos kvinnor något större än hos män.
Vanligtvis har en person två par bisköldkörtlar (övre och nedre), belägna på baksidan av sköldkörteln, utanför dess kapsel, nära de övre och nedre polerna. Antalet och lokaliseringen av bisköldkörtlarna kan dock variera; ibland finns upp till 12 bisköldkörtlar. De kan vara belägna i sköldkörtelns och tymusvävnaden, i främre och bakre mediastinum, i hjärtsäcken, bakom matstrupen, i området för halspulsåderns bifurkation. De övre bisköldkörtlarna har formen av en tillplattad äggform, de nedre är sfäriska. Deras dimensioner är ungefär från 6x3 till 4x1,5 - 3 mm, den totala vikten är från 0,05 till 0,5 g, färgen är rödaktig eller gulbrun. Blodtillförseln till bisköldkörtlarna sker huvudsakligen genom grenarna av den nedre sköldkörtelartären, venöst utflöde sker genom venerna i sköldkörteln, matstrupen och luftstrupen. Bisköldkörtlarna innerveras av sympatiska fibrer i de återkommande och övre larynxnerverna, medan parasympatisk innervation utförs av vagusnerverna. Bisköldkörtlarna är täckta av en tunn bindvävskapsel; från den sträcker sig septa in i körtlarna. De innehåller blodkärl och nervfibrer. Bisköldkörtlarnas parenkym består av paratyrocyter, eller huvudceller, bland vilka man, beroende på färgningsgraden, urskiljer hormonellt aktiva ljusa eller glänsande celler, såväl som vilande mörka celler. Huvudcellerna bildar kluster, snören och kluster, och hos äldre - folliklar med kolloid i håligheten. Hos vuxna uppträder celler, huvudsakligen belägna längs periferin av bisköldkörtlarna, färgade med eosin - eosinofila eller oxyfila celler, som är degenererande huvudceller. I bisköldkörtlarna kan man också hitta övergångsformer mellan huvud- och oxyfila celler.
De första framgångarna med att klargöra syntesfrågorna, avkoda strukturen och studera metabolismen av paratyreoideahormon uppnåddes efter 1972. Paratyreoideahormon är en enkelkedjig polypeptid bestående av 84 aminosyrarester, utan cystein, med en molekylvikt på cirka 9500 dalton, bildad i bisköldkörtlarna från en bioprekursor - proparatyreoideahormon (proPTH), som har 6 ytterligare aminosyror vid NH2 änden. ProPTH syntetiseras i bisköldkörtlarnas huvudceller (i deras granulära endoplasmatiska retikulum) och omvandlas till bisköldkörtelhormon i processen för proteolytisk klyvning i Golgi-apparaten. Dess biologiska aktivitet är signifikant lägre än PTH:s aktivitet. Tydligen saknas proPTH i blodet hos friska personer, men vid patologiska tillstånd (med adenom i bisköldkörtlarna) kan det utsöndras i blodet tillsammans med PTH. Nyligen upptäcktes en prekursor till proPTH, preproPTH, som innehåller ytterligare 25 aminosyrarester vid NH2-terminalen. Således innehåller preproPTH 115 aminosyrarester, proPTH - 90 och PTH - 84.
Strukturen hos bovint och porcint paratyreoideahormon har nu fastställts helt. Humant paratyreoideahormon har isolerats från bisköldkörteladenom, men dess struktur har endast delvis klarlagts. Det finns skillnader i strukturen hos paratyreoideahormon, men djur- och humana paratyreoideahormoner uppvisar korsimmunreaktivitet. Polypeptiden som består av de första 34 aminosyraresterna behåller praktiskt taget den biologiska aktiviteten hos det naturliga hormonet. Detta gör att vi kan anta att de återstående nästan % av molekylen vid karboxyländen inte är direkt relaterade till de huvudsakliga effekterna av paratyreoideahormon. Fragment 1-29 av paratyreoideahormon uppvisar också en viss biologisk och immunologisk aktivitet. Biologiskt inaktivt fragment 53-84 uppvisar också en immunologisk effekt, dvs. dessa egenskaper hos paratyreoideahormon uppvisas av minst två sektioner av dess molekyl.
Det bisköldkörtelhormon som cirkulerar i blodet är heterogent och skiljer sig från det nativa hormonet som utsöndras av bisköldkörtlarna. Minst tre olika typer av bisköldkörtelhormon urskiljs i blodet: intakt bisköldkörtelhormon med en molekylvikt på 9 500 dalton; biologiskt inaktiva substanser från karboxyldelen av bisköldkörtelhormonmolekylen med en molekylvikt på 7 000–7 500 dalton; biologiskt aktiva substanser med en molekylvikt på cirka 4 000 dalton.
Ännu mindre fragment hittades i venöst blod, vilket indikerar att de bildades i periferin. De huvudsakliga organen där fragment av paratyreoideahormon bildades var lever och njurar. Fragmenteringen av paratyreoideahormon i dessa organ var ökad vid leverpatologi och kronisk njursvikt (CRF). Under dessa förhållanden stannade fragment av paratyreoideahormon kvar i blodomloppet betydligt längre än hos friska individer. Levern absorberade huvudsakligen intakt paratyreoideahormon, men avlägsnade varken karboxylterminala eller aminoterminala paratyreoideahormonfragment från blodet. Njurarna spelade en ledande roll i metabolismen av paratyreoideahormon. De stod för nästan 60 % av den metaboliska clearance av karboxylterminalt immunreaktivt hormon och 45 % av det aminoterminala fragmentet av paratyreoideahormon. Det huvudsakliga metabolismområdet för det aktiva aminoterminala fragmentet av paratyreoideahormon var ben.
Pulserande utsöndring av paratyroidhormon observerades, mest intensiv på natten. Efter 3-4 timmar från början av nattens sömn är dess innehåll i blodet 2,5-3 gånger högre än den genomsnittliga dagtidsnivån.
Paratyreoideahormonets huvudsakliga funktion är att upprätthålla kalciumhomeostas. Samtidigt är serumkalcium (totalt och särskilt joniserat) den huvudsakliga regulatorn av paratyreoideahormonsekretion (en minskning av kalciumnivåerna stimulerar paratyreoideahormonsekretionen, medan en ökning hämmar den), dvs. regleringen sker enligt feedbackprincipen. Vid hypokalcemi ökar omvandlingen av proPTH till paratyreoideahormon. Magnesiumhalten i blodet spelar också en viktig roll i frisättningen av paratyreoideahormon (dess ökade nivå stimulerar, medan dess minskade nivå hämmar paratyreoideahormonsekretionen). Paratyreoideahormonets huvudmål är njurarna och skelettet, men effekten av paratyreoideahormon på kalciumabsorption i tarmen, kolhydrattolerans, serumlipidnivåer, dess roll i utvecklingen av impotens, hudklåda etc. är känd.
För att karakterisera effekten av parathyroidhormon på ben är det nödvändigt att ge kortfattad information om benvävnadens struktur, egenskaperna hos dess fysiologiska resorption och ombyggnad.
Det är känt att huvuddelen av kalciumet i kroppen (upp till 99 %) finns i benvävnad. Eftersom det finns i ben i form av fosfor-kalciumföreningar, finns även % av det totala fosforinnehållet i ben. Deras vävnad, trots sin skenbara statiska natur, ombyggs ständigt, är aktivt vaskulariserad och har höga mekaniska egenskaper. Ben är en dynamisk "depå" av fosfor, magnesium och andra föreningar som är nödvändiga för att upprätthålla homeostas i mineralmetabolismen. Dess struktur inkluderar täta mineralkomponenter som är nära besläktade med den organiska matrisen, som består av 90-95 % kollagen, små mängder mukopolysackarider och icke-kollagenproteiner. Mineraldelen av benet består av hydroxiapatit - dess empiriska formel är Ca10 (PO4) 6 (OH) 2 - och amorft kalciumfosfat.
Ben bildas av osteoblaster som härrör från odifferentierade mesenkymceller. Dessa är mononukleära celler som är involverade i syntesen av komponenter i den organiska benmatrisen. De är belägna i ett monolager på benytan och står i nära kontakt med osteoiden. Osteoblaster ansvarar för avsättningen av osteoiden och dess efterföljande mineralisering. Produkten av deras vitala aktivitet är alkaliskt fosfatas, vars innehåll i blodet är en indirekt indikator på deras aktivitet. Omgivna av mineraliserad osteoid omvandlas vissa osteoblaster till osteocyter - mononukleära celler, vars cytoplasma bildar kanaler associerade med kanalerna hos angränsande osteocyter. De deltar inte i benombyggnad, men är involverade i processen med perilacunar destruktion, vilket är viktigt för snabb reglering av kalciumnivåerna i blodserumet. Benresorption utförs av osteoklaster - jättelika polynukleära celler, tydligen bildade genom fusion av mononukleära makrofager. Det antas också att prekursorerna till osteoklaster kan vara hematopoetiska stamceller i benmärgen. De är rörliga och bildar ett lager i kontakt med benet, beläget i områden med dess största resorption. På grund av frisättningen av proteolytiska enzymer och surt fosfatas orsakar osteoklaster kollagennedbrytning, hydroxiapatitnedbrytning och avlägsnande av mineraler från matrisen. Nybildad dåligt mineraliserad benvävnad (osteoid) är resistent mot osteoklastisk resorption. Osteoblasternas och osteoklasternas funktioner är oberoende men samordnade med varandra, vilket leder till normal skelettombyggnad. Bentillväxt i längd beror på endokondral ossifikation, tillväxt i bredd och tjocklek på periosteal ossifikation. Kliniska studier med 47 Ca har visat att upp till 18 % av det totala kalciuminnehållet i skelettet förnyas varje år. När ben skadas (frakturer, infektiösa processer) resorberas det förändrade benet och nytt ben bildas.
Cellkomplex som är involverade i den lokala processen för benresorption och -bildning kallas basala multicellulära ombyggnadsenheter (BMU). De reglerar den lokala koncentrationen av kalcium, fosfor och andra joner, syntesen av organiska komponenter i benet, särskilt kollagen, dess organisation och mineralisering.
Den huvudsakliga effekten av paratyreoideahormon i skelettet är att förbättra resorptionsprocesserna, vilket påverkar både mineral- och organiska komponenter i benstrukturen. Paratyreoideahormon främjar tillväxten av osteoklaster och deras aktivitet, vilket åtföljs av en förstärkt osteolytisk effekt och en ökning av benresorptionen. I detta fall löses hydroxiapatitkristallerna upp med frisättningen av kalcium och fosfor i blodet. Denna process är den huvudsakliga mekanismen för att öka kalciumnivån i blodet. Den består av tre komponenter: mobilisering av kalcium från det perilakunära benet (djupa osteocyter); proliferation av osteoprogeneratorceller till osteoklaster; upprätthållande av en konstant kalciumnivå i blodet genom att reglera dess frisättning från benet (ytliga osteocyter).
Således ökar paratyroidhormon initialt aktiviteten hos osteocyter och osteoklaster, vilket förstärker osteolysen, vilket orsakar en ökning av kalciumnivån i blodet och ökad utsöndring av kalcium och oxyprolin i urinen. Detta är den första, kvalitativa, snabba effekten av paratyroidhormon. Den andra effekten av paratyroidhormon på benen är kvantitativ. Den är förknippad med en ökning av poolen av osteoklaster. Vid aktiv osteolys sker en stimulans för ökad proliferation av osteoblaster, både resorption och benbildning med en övervägande resorption aktiveras. Vid ett överskott av paratyroidhormon uppstår en negativ benbalans. Detta åtföljs av överdriven utsöndring av oxyprolin - en produkt av kollagennedbrytning och sialinsyror som ingår i strukturen av mukopolysackarider. Paratyroidhormon aktiverar cykliskt adenosinmonofosfat (cAMP). Ökad utsöndring av cAMP i urinen efter administrering av paratyroidhormon kan fungera som en indikator på vävnadskänslighet för det.
Den viktigaste effekten av paratyreoideahormon på njurarna är dess förmåga att minska fosforreabsorptionen, vilket ökar fosfati. Mekanismen för reduktionen i olika delar av nefronet är olika: i den proximala delen beror denna effekt av paratyreoideahormon på ökad permeabilitet och sker med deltagande av cAMP, medan den i den distala delen inte är beroende av cAMP. Den fosfatitiska effekten av paratyreoideahormon förändras med vitamin D-brist, metabolisk acidos och minskat fosforinnehåll. Paratyreoideahormoner ökar den totala tubulära reabsorptionen av kalcium något. Samtidigt minskar det den i de proximala delarna och ökar den i de distala delarna. Det senare är av dominerande betydelse - paratyreoideahormon minskar kalciumclearance. Paratyreoideahormon minskar den tubulära reabsorptionen av natrium och dess bikarbonat, vilket kan förklara utvecklingen av acidos vid hyperparatyreoidism. Det ökar bildandet av 1,25-dioxikolekalciferol 1,25(OH 2 )D 3 i njurarna - den aktiva formen av vitamin D 3. Denna förening ökar kalciumreabsorptionen i tunntarmen genom att stimulera aktiviteten hos ett specifikt kalciumbindande protein (CaBP) i dess vägg.
Den normala nivån av bisköldkörtelhormon är i genomsnitt 0,15–0,6 ng/ml. Det varierar beroende på ålder och kön. Den genomsnittliga halten av bisköldkörtelhormon i blodet hos personer i åldern 20–29 år är (0,245 ± 0,017) ng/ml, 80–89 år - (0,545 ± 0,048) ng/ml; nivån av bisköldkörtelhormon hos 70-åriga kvinnor är (0,728 ± 0,051) ng/ml, hos män i samma ålder - (0,466 ± 0,40) ng/ml. Således ökar halten av bisköldkörtelhormon med åldern, men i större utsträckning hos kvinnor.
Som regel bör flera olika tester användas för differentialdiagnos av hyperkalcemi.
Vi presenterar den kliniska och patogenetiska klassificeringen som vi utvecklat, baserad på klassificeringen av OV Nikolaev och VN Tarkaeva (1974).
Klinisk och patogenetisk klassificering av sjukdomar associerade med nedsatt utsöndring av paratyroidhormon och känslighet för det
Primär hyperparatyreoidism
- Genom patogenes:
- hyperfunktionella adenom;
- hyperplasi av OGD;
- hyperfunktionell bisköldkörtelcancer;
- multipel endokrin neoplasi typ I med hyperparatyreoidism (Wermers syndrom);
- multipel endokrin neoplasi typ II med hyperparatyreoidism (Sipple syndrom).
- Enligt kliniska egenskaper:
- benform:
- osteoporotisk,
- fibrocystisk osteit,
- "Pagetoid";
- visceropatisk form:
- med övervägande skador på njurarna, mag-tarmkanalen, neuropsykiatrisk sfär;
- blandad form.
- benform:
- Nedströms:
- kryddad;
- kronisk.
Sekundär hyperparatyreoidism (sekundär hyperfunktion och hyperplasi i bisköldkörtlarna med långvarig hypokalcemi och hyperfosfatemi)
- Njurpatologi:
- kronisk njursvikt;
- tubulopati (Albright-Fanconi-typ);
- njurrakit.
- Tarmpatologi:
- malabsorptionssyndrom.
- Benpatologi:
- senil osteomalaci;
- barnsängslig;
- idiopatisk;
- Pagets sjukdom.
- D-vitaminbrist:
- njursjukdom;
- lever;
- ärftliga enzymbrister.
- Maligna sjukdomar: myelom.
Tertiär hyperparatyreoidism
- Autonomat fungerande adenom i bisköldkörtlarna, som utvecklas mot bakgrund av långvarig sekundär hyperparatyreoidism.
Pseudohyperparatyreoidism
- Produktion av bisköldkörtelhormon av tumörer av icke-bisköldkörtelursprung.
Hormonellt inaktiva cystiska och tumörformationer i bisköldkörtlarna
- Cysta.
- Hormonellt inaktiva tumörer eller karcinom.
Hypoparatyreoidism
- Medfödd underutveckling eller frånvaro av bisköldkörtlarna.
- Idiopatisk, autoimmunt ursprung.
- Postoperativt, utvecklat i samband med borttagning av bisköldkörtlarna.
- Postoperativt på grund av nedsatt blodtillförsel och innervation.
- Strålskador, exogena och endogena (extern strålbehandling, behandling av sköldkörtelsjukdom med radioaktivt jod).
- Skada på bisköldkörtlarna på grund av blödning eller infarkt.
- Infektiösa lesioner.
Pseudohypoparatyreoidism
- Typ I - okänslighet hos målorganen för parathyroidhormon, beroende på adenylatcyklas;
- Typ II - målorganens okänslighet för paratyroidhormon, oberoende av adenylatcyklas, möjligen av autoimmunt ursprung.
Pseudopseudohypoparatyreoidism
Förekomsten av somatiska tecken på pseudohypoparatyreoidism hos friska släktingar i familjer till patienter med pseudohypoparatyreoidism utan karakteristiska biokemiska störningar och utan tetani.
 [ 13 ], [ 14 ], [ 15 ], [ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ], [ 21 ]
[ 13 ], [ 14 ], [ 15 ], [ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ], [ 21 ]

