Medicinsk expert av artikeln
Nya publikationer
Experimentella modeller för osteoartrit
Senast recenserade: 07.07.2025

Allt iLive-innehåll är mediekontrollerat eller faktiskt kontrollerat för att säkerställa så mycket faktuell noggrannhet som möjligt.
Vi har strikta sourcing riktlinjer och endast länk till välrenommerade media webbplatser, akademiska forskningsinstitut och, när det är möjligt, medicinsk peer granskad studier. Observera att siffrorna inom parentes ([1], [2] etc.) är klickbara länkar till dessa studier.
Om du anser att något av vårt innehåll är felaktigt, omodernt eller på annat sätt tveksamt, välj det och tryck på Ctrl + Enter.
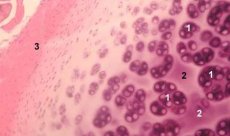
Brosk är en högspecialiserad vävnad som endast innehåller en typ av celler (kondrocyter) och kännetecknas av avsaknaden av blod och lymfkärl. Brosk får huvudsakligen näring genom absorption från synovialvätskan. Kondrocyternas metabolism regleras av ett antal lösliga faktorer som produceras lokalt av kondrocyter och omgivande vävnader. Kondrocyternas funktion beror också på den extracellulära miljöns sammansättning (syretryck, jonkoncentration, pH, etc.), sammansättningen av ECM, interaktionen mellan celler och matris, samt fysiska signaler. Huvudsyftet med experimentell modellering är att skapa kulturer i den extracellulära miljön utan att förändra fenotypen hos mogna celler. Det andra målet är att skapa kulturer för att studera kondrocyternas för tidiga, fördröjda, kortsiktiga eller förlängda svar på kemiska och/eller fysiska signaler. In vitro-studier ger också en möjlighet att studera kondrocyternas beteende vid artros. Det tredje målet är att utveckla samodlingssystem som möjliggör studier av interaktionerna mellan olika vävnader i leden. Den fjärde uppgiften är förberedelse av broskimplantat för efterföljande transplantation. Och slutligen är den femte uppgiften studiet av tillväxtfaktorer, cytokiner eller terapeutiska medel som kan stimulera reparation och/eller hämma broskresorption.
Under de senaste decennierna har olika modeller av cellkulturer av ledbrosk skapats, inklusive monolagerkulturer, suspenderade kulturer, kondronkulturer, explantat, samkulturer och odödliga cellkulturer. Varje kultur har sina egna fördelar och nackdelar, och var och en är lämplig för att studera en specifik aspekt av kondrocytmetabolism. Således är broskexplantat en utmärkt modell för att studera omsättningen av matrixelement, vilket kräver genuina cellytereceptorer och normala cell-matrix- och matrix-cell-interaktioner. Samtidigt rekommenderas det att studera matrixavlagringar eller mekanismer som reglerar kondrocytmetabolism på en kultur av isolerade celler. En monolagerkultur med låg densitet är nödvändig för att studera processen för celldifferentiering. Kulturer suspenderade i en naturlig eller syntetisk matrix är en modell för att analysera kondrocyters adaptiva respons på mekanisk stress.
Kondrocytkulturer
Flera viktiga punkter bör beaktas vid val av broskvävnad för in vitro-studier. Matrixsammansättningen och den metaboliska aktiviteten hos kondrocyter varierar mellan leder, och det senare beror också på djupet av kondrocyternas placering i vävnaden. Dessa data erhölls i flera experiment där isolerade kondrocytsubpopulationer från broskzoner med olika djup studerades. Ett antal morfologiska och biokemiska skillnader hittades mellan odlade kondrocyter belägna i de ytliga och djupa lagren av ledbrosk. Ytliga celler syntetiserar en gles, proteoglykanfattig fibrillär matris, medan djupare celler producerar en matris rik på fibriller och proteoglykaner. Dessutom producerar ytliga celler relativt fler små icke-aggregerade proteoglykaner och hyaluronsyra och relativt mindre aggrekan och keratansulfat än djupare kondrocyter. Ett annat viktigt utmärkande drag hos metabolismen hos kondrocyter isolerade från broskzoner med olika djup är responsen på en exogen stimulus. Enligt M. Aydelotte et al. var bovina kondrocyter från den ytliga zonen av brosk känsligare för IL-1 än celler från den djupa zonen.
Cellbeteendet beror också på vävnadens placering. Kondrocyter från revbens- och öronbrosk från samma djur reagerar olika på tillväxtfaktorer som fibroblasttillväxtfaktor (FGF) och TGF-beta. FGF ökade inkorporeringen av tymidin, prolin och leucin i odlade revben men inte i öronkondrocyter. TGF-beta ökade inkorporeringen av tymidin i revbens- och öronbroskkondrocyter men hade ingen effekt på inkorporeringen av tymidin och prolin i öronkondrocyter. Broskceller från områden med hög stress skiljer sig från de från områden med låg stress på brosket. Således syntetiserar kondrocyter från knäledsbrosk från mogna får från den centrala regionen av skenbenets ledyta som inte täcks av menisken, vilken bär den största belastningen in vivo, mindre aggrecan, men mer dekorin än celler från de zoner som täcks av menisken. Författarna betonar också vikten av att använda brosk från identiska ledzoner när man studerar ledernas syntetiska funktion.
Kondrocyters metabolism och deras respons på reglerande faktorer beror också i hög grad på givarens ålder, deras skelettutveckling och tillståndet hos de leder från vilka cellerna tas. Hos humana kondrocyter observeras en signifikant minskning av det proliferativa svaret med åldern. Den största minskningen observeras hos givare i åldern 40-50 år och över 60 år. Dessutom minskar svårighetsgraden av det proliferativa svaret på tillväxtfaktorer (t.ex. FGF och TGF-beta) med åldrandet. Förutom kvantitativa förändringar i kondrocytproliferation finns det också kvalitativa förändringar. Celler från unga givare (10-20 år) svarar bättre på trombocytderiverad tillväxtfaktor (PDGF) än på TGF-beta, medan motsatsen observeras i celler från vuxna givare. Flera mekanismer används för att förklara åldersberoende förändringar i kondrocyters syntetiska funktion och deras respons på tillväxtfaktorer. Dessa inkluderar en minskning av antalet och affiniteten hos ytcellreceptorer, förändringar i syntesen och bioaktiviteten hos tillväxtfaktorer och cytokiner, samt modifiering av postreceptorsignaler.
Patologiska tillstånd i lederna förändrar också morfologin och den metaboliska aktiviteten hos kondrocyter. Således identifierade J. Kouri et al. (1996) tre delpopulationer av kondrocyter i brosk vid artros. Kondrocyter från den ytliga och övre delen av mitten av brosket bildar kluster och syntetiserar en större mängd proteoglykaner och kollagen. TGF-beta och insulinliknande tillväxtfaktor (IGF) kan stimulera syntesen av proteoglykaner av kondrocyter och delvis neutralisera effekterna av IL-1 och TNF-α. Explantat av brosk som påverkats av artros och kondrocyter isolerade från brosket hos en patient med artros är mer känsliga för stimulering av TGF-beta än kondrocyter från friskt brosk. Dessa skillnader är troligtvis förknippade med fenotypiska förändringar i kondrocyter i de övre lagren av ledbrosk.
Isolering av individuella kondrocyter uppnås genom sekventiell behandling av ECM med proteolytiska enzymer. Efter att de frisatts från ECM är de isolerade cellerna idealiska för att studera de novo-syntesen av matrixkomponenter. Vissa författare använder endast klostridialkollagenas, medan andra förinkuberar brosket med trypsin, pronas, DNas och/eller hyaluronidas. Antalet isolerade celler beror på vilka enzymer som används. Således kan 1,4–10⁶ kondrocyter erhållas från 1 g vävnad vid behandling med enbart kollagenas, medan pronas, hyaluronidas och kollagenas används – 4,3–10⁶ . Vid behandling med kollagenas kvarstår aggrekan, proteiner, IL-6 och IL-8 i cellkulturen i betydligt större mängder än vid sekventiell behandling med olika enzymer. Det finns flera förklaringar till dessa skillnader mellan de två cellkulturerna:
- Cellreceptorer skadas eller hämmas av enzymer, TGF-beta hämmar DNA- och proteoglykansyntes i nyligen isolerade kondrocyter (dag 1), medan DNA- och proteoglykansyntes i kondrocyter odlade i ett monolager (7 dagar) stimuleras av TGF-beta. Emellertid krävs en tillräcklig period för återuttryck av dessa membrankomponenter innan experimentet påbörjas.
- Exogena proteaser kan störa den integrinmedierade cell-matrixinteraktionen. Integrinfamiljen främjar kondrocyters bindning till ECM-molekyler (Shakibaei M. et al., 1997). Denna störning kan påverka uttrycket av matrixgener.
- Resterna av matrixkomponenter kan reglera kondrocyters syntetiska funktion. Integriner kan känna igen produkterna från ECM-nedbrytning och spelar därmed en viktig roll i vävnadsreparation efter proteolytiska enzymers verkan. T. Larsson et al. (1989) rapporterade att tillsatsen av intakta eller fragmenterade proteoglykaner till cellkultur stimulerar syntesen av proteiner och proteoglykaner. Emellertid orsakar en hög nivå av hyaluronsyra en signifikant minskning av inkluderingen av sulfater i syntesen av proteoglykaner av kondrocyter från kycklingembryon, mogna kondrocyter från gris- och råttkondrosarkomceller. Dessutom är hyaluronsyra en hämmare av proteoglykanfrisättning från celler även i närvaro av IL-1b, TNF-α, FGF, vilket indikerar motverkan av den första biologiska aktiviteten hos tillväxtfaktorer och cytokiner. Den exakta mekanismen bakom hyaluronsyrans verkan är fortfarande oklar; kondrocyter är kända för att innehålla en receptor för hyaluronsyra associerad med aktinfilament i cytosolen. Bindning av hyaluronsyra till dess receptor stimulerar proteinfosforylering. Dessa data visar således modulering av kondrocyternas metaboliska funktion av fragmenterade eller nativa molekyler av matrixproteiner genom aktivering av cellmembranreceptorer.
- Snabb stimulering av matrixproteinsyntes av kondrocyter med enzymer kan vara en konsekvens av förändringar i kondrocyternas form och/eller cytoskelettal omorganisation.
- Vissa cytokiner (t.ex. IL-8) och tillväxtfaktorer (t.ex. IGF-1, TGF-β) sekvestreras i ECM. Det mest kända exemplet är bindningen av TGF-β av dekorin, vilket resulterar i en minskad förmåga hos den förra att inducera celltillväxt i kinesiska hamsteräggstocksceller. Upptäckten att dekorinhalten i brosk ökar med åldern tyder på en minskning av TGF-β-biotillgängligheten med åldrande. Tillväxtfaktorer och cytokiner kan frisättas från matrixrester under odling och därefter modulera kondrocytfunktionen.
Monolagerkultur av kondrocyter
Den differentierade fenotypen hos kondrocyter kännetecknas främst av syntesen av typ II-kollagen och vävnadsspecifika proteoglykaner, samt en låg nivå av mitotisk aktivitet. Det finns bevis för att kondrocyter, vid långvarig cellodling i ett monolager, såväl som efter flera upprepade cellpassager, förlorar sina sfäriska konturer och får en långsträckt, fibroblastliknande form. Med sådan fibroblastisk metaplasi modifieras även cellernas syntetiska funktion, kännetecknad av en progressiv minskning av syntesen av kollagen typ II, IX och XI och en ökning av syntesen av kollagen typ I, III och Y. Små icke-aggregerade proteoglykaner syntetiseras på grund av funktionell aggrekan. Syntesen av katepsin B och L är extremt låg i differentierade celler, men ökar i processen med förlust av differentiering. Kollagenas-1 uttrycks i differentierade kondrocyter; med långvarig odling minskar dess uttryck, medan produktionen av vävnadshämmare av metalloproteaser (TIMP) ökar.
Differentierade kondrocyter återuttrycker kollagen av den differentierade fenotypen när de överförs från monolager till suspenderad kultur. Differentieringsprocessen är förmodligen relaterad till cellformen. Denna egenskap används regelbundet av forskare som studerar defekta transplantat med autologa kondrocyter. Ett litet antal celler erhållna från biopsimaterial kan expanderas i monolagerkultur och sedan återinföras i en tredimensionell matris före transplantation. Återuttryck av en specifik fenotyp av dedifferentierade kondrocyter som överförs till agaroskultur kan stimuleras av TGF-β, ossein-hydroxiapatitkomplex och askorbinsyra.
Som svar på tillväxtfaktorer och cytokiner modifieras kondrocyter under differentieringsprocessen. Det cellulära svaret på cytokiner och tillväxtfaktorer skiljer sig mellan odifferentierade och differentierade kondrocyter. IL-1 stimulerar fibroblastproliferation, medan tillväxten av odifferentierade kondrocyter hämmas av IL-1. DNA-syntes stimuleras av IGF-1 i förlängda men inte tillplattade kondrocyter. I differentierade kondrocyter är de stimulerande effekterna av IL-1beta och TNF-α på prokollagenasproduktion mer uttalade än i odifferentierade kondrocyter.
Kondrocytodling
Odling av kondrocyter i suspension i ett flytande medium eller i en naturlig eller syntetisk tredimensionell matris stabiliserar kondrocytfenotypen. Cellerna behåller sin sfäriska form och syntetiserar vävnadsspecifika proteiner. Suspenderad kultur av kondrocyter rekommenderas vanligtvis för att studera bildandet av en ny pericellulär matris. Kulturer av kondrocyter i syntetiska eller naturliga absorberande polymerer används för implantation av celler i broskdefekter för att stimulera regenerering av ledbroskvävnad. Det syntetiska eller naturliga mediet för implanterade celler måste uppfylla ett antal krav:
- implantat måste ha en porös struktur för cellvidhäftning och tillväxt,
- Varken polymeren i sig eller dess nedbrytningsprodukter bör orsaka inflammation eller toxiska reaktioner vid implantation in vivo,
- Transplantatbäraren måste ha förmågan att binda till intilliggande brosk eller subkondralt ben,
- den naturliga eller syntetiska matrisen måste ha förmåga att absorbera, dess nedbrytning måste balanseras genom vävnadsregenerering,
- För att underlätta broskreparation måste matrisens kemiska struktur och porarkitektur underlätta upprätthållandet av den cellulära fenotypen och syntesen av vävnadsspecifika proteiner av de kondrocyter som placeras i den,
- Under in vivo-implantation är det nödvändigt att studera de mekaniska egenskaperna hos den syntetiska eller naturliga matrisen.
 [ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ]
[ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ]
Suspension av kondrocyter i flytande fas
Cellers vidhäftning till plastkärl i vilka kondrocyter odlas kan förhindras genom att belägga deras väggar med en lösning av metylcellulosa, agaros, hydrogel (poly-2-hydroxietylmetakrylat) eller en kollagen-agarosblandning. Under dessa förhållanden bildar kondrocyter kluster och syntetiserar huvudsakligen aggrekan och vävnadsspecifika kollagener (II, IX, XI typer). Två typer av celler finns vanligtvis. Cellerna i mitten behåller en sfärisk form och är omgivna av en välutvecklad ECM, vilket bekräftas av histokemiska och ultrastrukturella studier. I periferin har kondrocyter skivformade konturer och är omgivna av en gles ECM; lite är känt om de funktionella egenskaperna hos sådana celler.
Det är möjligt att odla kondrocyter på mikrobärare som hålls i suspension; dextrankulor (cytodex), kollagenbelagda dextrankulor (cytodex III) och icke-porösa mikrosfärer av typ I-kollagen (cellagen) används som mikrobärare. Under dessa odlingsförhållanden fäster kondrocyter på mikrobärarens yta, behåller sin sfäriska form och producerar ett matrisliknande material. Dessutom främjar användningen av cellagen kondrocytproliferation och återuttryck av den normala fenotypen. Därför kan odling av kondrocyter på cellagenmikrosfärer användas för att återställa cellfenotypen före transplantation.
En annan metod för att odla kondrocytsuspensioner i flytande medium är deras odling i form av täta bollar bestående av celler (0,5-1 * 10 b ), erhållna genom centrifugering. Sådana kondrocyter kan producera en matris innehållande en stor mängd proteoglykaner, kollagen typ II, men inte kollagen typ I, vilket bekräftas med histologiska, immunhistokemiska och kvantitativa metoder.
Suspension av kondrocyter i naturlig ECM
Kondrocyter kan odlas i suspension i en tredimensionell matris (mjuk agar, agaros, kollagengel eller svamp, hyaluronsyra, fibrinlim, alginatkulor).
Kondrocyter odlade i agaros behåller sin normala fenotyp och syntetiserar typ II-kollagen och vävnadsspecifika aggrekanaggregat. Vid odling i agaros frisätts proteoglykaner som syntetiserats av cellen i mediet under 50 dagar. Som jämförelse är cellfasen i en monolagerkultur överfylld med glykosaminoglykaner redan under de första 5-6 dagarna av odlingen; vid odling i mediet sker en tidsberoende minskning efter ökad syntes och frisättning av glykosaminoglykaner under de första 8-10 dagarna. Icke desto mindre skiljer sig kondrocyternas beteende vid odling i agaros från det in vivo. I agaros innehåller ett stort antal syntetiserade aggrekanaggregat mindre molekyler och färre molekyler än in vivo. TGF-β stimulerar proteoglykansyntesen i explantatet, men minskar aggrekansyntesen i agaros.
Alginat är en linjär polysackarid som utvinns ur brunt alger. I närvaro av tvåvärda katjoner, såsom Ca2 + -joner, blir denna polymer en gel. Varje kondrocyt som är fångad i alginat är omgiven av en matris av negativt laddade polysackarider, vars porer är jämförbara med de i hyalint brosk. Matrisen som bildas av kondrocyter i alginatkulor består av två kompartment - ett tunt lager av cellassocierad matris motsvarande den pericellulära och territoriella matrisen i ledbrosk och en mer avlägsen matris motsvarande den interterritoriella i nativ vävnad. På den 30:e odlingsdagen är den relativa och absoluta volymen som upptas av cellerna och vart och ett av de två kompartmenten i en alginatkula nästan helt identisk med den i nativt brosk. Under nästan 30 dagar behåller kondrocyter sin sfäriska form och producerar aggrekan, vars hydrodynamiska egenskaper liknar de hos aggrekanmolekyler i ledbroskmatrisen, såväl som kollagenmolekyler av typerna II, IX och XI. Samtidigt, liksom andra suspensionskulturer, finns tillplattade celler på ytan av alginatkulor, vilka producerar en liten mängd kollagenmolekyler av typ I, vilka frisätts direkt i mediet och inte inkorporeras i ECM. Måttlig proliferation av kondrocyter observeras i alginatkulor. Efter 8 månaders odling i alginatgel förlorar mogna kondrocyter inte metabolisk aktivitet och fortsätter att syntetisera vävnadsspecifikt kollagen typ II och aggrecan.
H. Tanaka et al. (1984) undersökte diffusionsegenskaperna hos olika naturliga molekyler i alginat och fann att molekyler större än 70 kDa inte diffunderade genom alginat. Cellodling i alginat är därför lämplig för att studera regleringen av matrixbiosyntes och ECM-organisation. Tillgången till celler odlade i alginat gör det möjligt att studera verkan av peptidreglerande faktorer och farmakologiska medel på transkriptionell, posttranskriptionell och translationell nivå.
Kondrocyter odlas också i en matris av kollagenfibrer av typ I och II. S. Nehrer et al. (1997) jämförde funktionen hos hundkondrocyter i porösa kollagen-proteoglykanpolymermatriser innehållande kollagener av olika typer. De fann viktiga skillnader i morfologin för den biosyntetiska funktionen hos kondrocyter odlade i kollagenmatriser innehållande kollagen av typ I och II. Celler i en matris av kollagen typ II behöll sin sfäriska form, medan de i kollagen typ I hade en fibroblastliknande morfologi. Dessutom producerade kondrocyter i en matris av kollagen typ II en större mängd glykosaminoglykaner. J. van Susante et al. (1995) jämförde egenskaperna hos kondrocyter odlade i alginat- och kollagengel (typ I). Författarna fann en signifikant ökning av antalet celler i kollagengelen, men från den sjätte dagen av odlingen förlorade cellerna sin karakteristiska fenotyp och förvandlades till fibroblastliknande celler. I alginatgelen observerades en minskning av antalet celler, men kondrocyterna behöll sin normala fenotyp. I kollagengelen var antalet proteoglykaner per cell signifikant högre än i alginat, men i gelen observerades en minskning av syntesen av matrixelement, med början från den sjätte odlingsdagen, medan syntesen fortsatte att öka i alginat.
En fast tredimensionell fibrinmatris är en naturlig substans som stödjer kondrocyter suspenderade i den i en differentierad fenotyp. Tredimensionell fibrinmatris kan också användas som bärare vid kondrocyttransplantation. Fördelarna med fibrin är avsaknaden av cytotoxicitet, förmågan att fylla utrymme och vidhäftningsförmåga. Histologiska och biokemiska studier, autoradiografi och elektronmikroskopi har visat att kondrocyter i fibringel behåller sin morfologi, prolifererar och producerar matrix även efter 2 veckors odling. G. Homminga et al. (1993) rapporterade dock att fibrinsönderfall börjar efter 3 dagars odling och att kondrocytdedifferentieringen fortskrider.
Suspension av kondrocyter i artificiell (syntetisk) ECM
Broskimplantat för rekonstruktiv eller ortopedisk kirurgi kan erhållas genom att odla isolerade kondrocyter in vitro i en syntetisk biokompatibel matrix.
Kondrocyter odlade i polyglykolsyra prolifererar och bibehåller normal morfologi och fenotyp i 8 veckor. Kondrocyt-polyglykolsyrakomplexet består av celler, glykosaminoglykaner, kollagener och har en extern kollagenkapsel. Sådana implantat innehåller dock två typer av kollagenmolekyler - I och II. Implantat från kondrocyter som dedifferentierats genom en serie passager har en större mängd glykosaminoglykaner och kollagener än implantat från primärt odifferentierade kondrocyter.
L. Freed et al. (1993b) jämförde beteendet hos humana och bovina kondrocytkulturer i fibrös polyglykolsyra (FPGA) och porös polymjölksyra (PPLA). Efter 6–8 veckors odling av bovina kondrocyter i FPGA eller PPLA observerade författarna cellproliferation och regenerering av broskmatrisen. I FPGA hade kondrocyterna en sfärisk form och var belägna i lakuner omgivna av en broskmatris. Efter 8 veckors in vitro-odling innehöll den regenererade vävnaden upp till 50 % torrsubstans (4 % cellmassa, 15 % glykosaminoglykaner och 31 % kollagener). I PPLA hade cellerna en spindelformad form och en liten mängd glykosaminoglykaner och kollagen. I FPGA var celltillväxten 2 gånger mer intensiv än i PPLA. In vivo producerade kondrocyter odlade i VPGK och PPLC vävnad som histologiskt liknade brosk inom 1–6 månader. Implantaten innehöll glykosaminoglykaner, kollagener typ I och II.
Bovina fetala kondrocyter odlades i porös högdensitets hydrofob och hydrofil polyeten. Efter 7 dagars inkubation i båda substraten behöll cellerna en sfärisk form och innehöll huvudsakligen typ II-kollagen. Efter 21 dagars odling fann man att den hydrofila matrisen innehöll mer typ II-kollagen än den hydrofoba matrisen.
Broskvävnad kan också erhållas genom odling i ett monolager på Millicell-CM-filter. Förbeläggning av filtren med kollagen är nödvändig för fästandet av kondroitiner. Histologisk undersökning av kulturen visar ackumulering av kondrocyter i ECM innehållande proteoglykaner och typ II-kollagen. Typ I-kollagen detekterades inte i en sådan kultur. Kondrocyter i den erhållna broskvävnaden är sfäriska till formen, men på vävnadsytan är de något tillplattade. Tjockleken på den nybildade vävnaden ökade med tiden och berodde på cellmonolagrets initiala densitet. Under optimala odlingsförhållanden nådde broskvävnadens tjocklek 110 μm, organisationen av dess celler och kollagen i ytliga och djupa lager liknar den hos ledbrosk. ECM innehåller ungefär 3 gånger mer kollagen och proteoglykaner. Efter 2 veckors odling observerades matrixackumulering, vilket gjorde att vävnaden kunde extraheras från filtret och användas för transplantation.
Sims et al. (1996) studerade odling av kondrocyter i polyetylenoxidgel, en inkapslad polymermatris som möjliggör överföring av ett stort antal celler genom injektion. Sex veckor efter injektion i den subkutana vävnaden hos atymiska möss bildades nytt brosk, vilket morfologiskt karakteriserades av en vit opalescens liknande hyalint brosk. Histologiska och biokemiska data indikerade närvaron av aktivt prolifererande kondrocyter som producerar ECM.
Explantation
Explantation av broskvävnad används för att studera processerna för ana- och katabolism i den, upprätthållande av homeostas, resorption och reparation. Kondrocyter i broskexplantat upprätthåller en normal fenotyp och ECM-sammansättning liknande de i ledbrosk in vivo. Efter 5 dagars odling i närvaro av serum uppnås en konstant nivå av syntes och naturliga nedbrytningsprocesser. Vävnadsresorption kan accelereras i huvudkulturen och i kultur med tillsats av serum med hjälp av ett antal medel, såsom IL-IB, TNF-a, bakteriella lipopolysackarider, retinsyraderivat eller aktiva syreradikaler. För att studera broskreparation induceras dess skada av lösliga inflammatoriska mediatorer (H2O2 , IL 1, TNF-a) eller fysisk bristning av matrixen.
Den organotypiska odlingsmetoden är en modell för in vitro-studier av effekterna av isolerade externa faktorer på kondrocyter och den omgivande matrixen. In vivo är kondrocyter glest belägna i ECM och har inte kontakt med varandra. Den artikulära broskexplantationskulturen bevarar denna strukturella organisation, såväl som de specifika interaktionerna mellan kondrocyter och den omgivande extracellulära miljön. Denna modell används också för att studera effekterna av mekanisk stress, farmakologiska medel, tillväxtfaktorer, cytokiner och hormoner på broskmetabolismen.
En annan fördel med broskvävnadsexplantation är avsaknaden av skador på kondrocyter under inverkan av proteolytiska enzymer eller mekaniska faktorer, vilket är oundvikligt vid isolering av celler. Receptorer och andra membranproteiner och glykoproteiner skyddas från skadliga faktorer.
 [ 17 ], [ 18 ], [ 19 ], [ 20 ], [ 21 ]
[ 17 ], [ 18 ], [ 19 ], [ 20 ], [ 21 ]
Kondronkultur
Kondron är en strukturell, funktionell och metabolisk enhet i ledbrosk, bestående av en kondrocyt, dess pericellulära matrix och kompakta filamentösa kapsel, och ansvarig för matrixhomeostas. Kondroner extraheras mekaniskt från brosk och samlas in med hjälp av flera successiva låghastighetshomogeniseringar. Kondroner isolerade från zoner med olika broskdjup kan delas in i fyra kategorier: enstaka kondroner, parade kondroner, flera (tre eller fler) linjärt arrangerade kondroner (kondronkolonner) och kondronkluster.
Enskilda kondroner finns vanligtvis i de mellersta lagren av intakt brosk, parade kondroner finns vid gränsen mellan de mellersta och djupa lagren, linjärt arrangerade multipla kondroner är typiska för de djupa lagren av intakt brosk. Slutligen består kondronkluster av slumpmässigt organiserade grupper av enkla och parade kondroner, som behåller ett aggregerat tillstånd efter homogenisering. Kondronkluster är stora broskfragment, vanligtvis innehållande flera kondroner och radiellt arrangerade kollagenfibriller, dvs. en typisk organisation som är karakteristisk för de djupa lagren i matrisen. Kondroner är immobiliserade i transparent agaros, vilket möjliggör studier av deras struktur, molekylära sammansättning och metaboliska aktivitet. Kondron-agarossystemet anses vara en mikromodell av brosk, som skiljer sig från det traditionella kondrocyt-agarossystemet genom att den naturliga mikromiljön bevaras, och det finns inget behov av att syntetisera och montera den. Kondronkultur är en modell för att studera interaktionerna mellan celler och matris i ledbrosk under normala och patologiska förhållanden.
 [ 22 ], [ 23 ], [ 24 ], [ 25 ], [ 26 ], [ 27 ]
[ 22 ], [ 23 ], [ 24 ], [ 25 ], [ 26 ], [ 27 ]
Kultur av odödliga kondrocyter
Rekombinant DNA eller onkogeninnehållande virus som kan göra en cell "odödlig" används för att skapa permanenta cellinjer. Odödliga kondrocyter har förmågan att proliferera oändligt samtidigt som de bibehåller en stabil fenotyp. F. Mallein-Gerin et al. (1995) visade att SV40T-onkogenen inducerar proliferation av muskondrocyter, som fortsätter att stabilt uttrycka kollagen av typ II, IX och XI, såväl som artikulärt aggrekan och bindande protein. Emellertid förvärvar en sådan cellinje förmågan att syntetisera kollagen av typ I när den odlas i en monolagerkultur eller i en agarosgel.
W. Horton et al. (1988) beskrev en linje av odödliga celler med låg uttrycksnivå av typ II-kollagen mRNA. Dessa celler erhölls genom transformation med ett musretrovirus innehållande I-myc- och y-ra-onkogener. Denna typ av celler representerar en unik modell för att studera interaktionerna i den artikulära matrisen i frånvaro av typ II-kollagen, såväl som regleringen av typ II-kollagensyntes.
Odling av kondropriter med muterade eller deleerade gener är en bekväm modell för att studera deras fysiologiska funktion. Denna modell är särskilt lämplig för att studera rollen av specifika molekyler i organisationen av broskmatrixen eller för att undersöka effekterna av olika reglerande faktorer på broskmetabolismen. Kondrocyter med en deleerad gen för typ IX-kollagen syntetiserar kollagenfibriller som är bredare än normalt, vilket indikerar att typ IX-kollagen reglerar fibrillernas diameter. Som nämnts i kapitel 1 har en mutation i COLAI-genen som kodar för typ II-kollagen nyligen upptäckts i familjer med primär generaliserad artros. För att studera effekten av mutant typ II-kollagen på den artikulära matrisen transfekterade R. Dharmrvaram et al. (1997) (infekterade med främmande nukleinsyra) defekta COL 2 AI (arginin vid position 519 är ersatt av cystein) in i humana fetala kondrocyter in vitro.
Samkultursystem. I leden interagerar brosk med andra typer av celler som finns i synovialmembranet, synovialvätskan, ligamenten och det subkondrala benet. Kondrocyternas metabolism kan påverkas av olika lösliga faktorer som syntetiseras av de listade cellerna. Vid artrit förstörs således ledbrosk av proteolytiska enzymer och fria radikaler som produceras av synovialceller. Därför har modeller utvecklats för att studera komplexa interaktioner mellan brosk och omgivande vävnader, vilka kallas samkulturer.
S. Lacombe-Gleise et al. (1995) odlade kaninkondrocyter och osteoblaster i ett samodlingssystem (COSTAR) där cellerna separerades av ett mikroporöst membran (0,4 μm) vilket möjliggjorde utbyte mellan de två celltyperna utan direkt kontakt. Denna studie visade osteoblasters förmåga att stimulera kondrocyttillväxt via lösliga mediatorer.
AM Malfait och medförfattare (1994) studerade sambandet mellan perifera blodmonocyter och kondrocyter. Denna modell är lämplig för att studera cytokinmedierade processer vid inflammatoriska artropatier (reumatoid artrit, seronegativa spondyloartritider, etc.). Författarna till modellen separerade cellerna med ett proteinbindande membran med porer på 0,4 μm i diameter. Studien visade att monocyter stimulerade med lipopolysackarid producerade IL-1 och TNF-α, vilket hämmade syntesen av aggrekan av kondrocyter och bidrog till nedbrytningen av redan syntetiserade aggrekanaggregat.
K. Tada et al. (1994) skapade en samodlingsmodell där endotelceller i en kollagengel (typ I) placerades i en inre kammare separerad från den yttre kammaren, med kondrocyter placerade i den med ett filter med en porstorlek på 0,4 μm. I ett tillstånd av fullständig isolering från den yttre kammaren bildade humana endotelceller rör i en kollagengel i närvaro av EGF eller TGF-a. När båda typerna av celler odlades samtidigt hämmades TGF-a-beroende rörbildning av endotelceller. Hämningen av denna process av kondrocyter eliminerades delvis av anti-TGF-beta-antikroppar. Det kan antas att TGF-beta producerad av kondrocyter hämmar vaskulariseringen av själva brosket.
S. Groot et al. (1994) odlade samtidigt kondrocyter från de hypertrofiska och proliferativa zonerna i benet hos ett 16 dagar gammalt musfoster med bitar av hjärnvävnad. Efter 4 dagars odling observerades transdifferentiering av kondrocyter till osteoblaster och början av osteoidbildning. Efter 11 dagars odling hade en del av brosket ersatts av benvävnad och benmatrisen var delvis förkalkad. Vissa neuropeptider och neurotransmittorer som produceras av hjärnvävnad påverkar osteoblasternas metabolism eller har receptorer för dem. Bland dem finns noradrenalin, vasoaktiv intestinal peptid, kalcitonin-genrelaterad peptid, substans P och somatostatin. Bitar av hjärnvävnad som odlas tillsammans med kondrocyter kan producera några av de listade faktorerna som kan inducera processen för transdifferentiering av kondrocyter till osteoblaster.
 [ 28 ], [ 29 ], [ 30 ], [ 31 ], [ 32 ], [ 33 ]
[ 28 ], [ 29 ], [ 30 ], [ 31 ], [ 32 ], [ 33 ]
Inverkan av externa faktorer på kondrocytodling
Syretryckets inverkan på kondrocyternas metabolism
I de flesta fall utvecklas kondrocytkulturer under förhållanden med atmosfärisk syretryck. Det är dock välkänt att kondrocyter in vivo existerar under hypoxiska förhållanden och att syretrycket varierar under olika patologiska förhållanden. Under mognaden observeras signifikanta förändringar i blodtillförseln till epifyserna. Eftersom vaskulariseringen varierar i olika zoner av tillväxtplattan varierar även syretrycket i dem. C. Brighton och R. Heppenstall (1971) visade att i kaninens tibialplatta är syretrycket i den hypertrofiska zonen lägre än i det omgivande brosket. Mätningar av vissa metaboliska parametrar visade att kondrocyter kan reagera snabbt på lokala förändringar i syrekoncentrationen. Först och främst minskar kondrocyternas förbrukning vid lågt syretryck. Med en minskning av syretrycket från 21 till 0,04 % ökar glukosutnyttjandet, aktiviteten hos glykolytiska enzymer och syntesen av mjölksyra ökar. Även vid lågt syretryck förblir den absoluta mängden ATP, ADP och AMP stabil. Dessa data indikerar att kondrocyternas metabolism syftar till maximal energibesparing. Emellertid förändras syntetisk aktivitet, och därmed reparationsprocesser, under hypoxiska förhållanden.
Högt syretryck påverkar också kondrocyternas metabolism, vilket orsakar en minskning av proteoglykan- och DNA-syntes och nedbrytning av broskmatrixen. Dessa effekter åtföljs vanligtvis av produktionen av fria syreradikaler.
Inverkan av jonkoncentration och osmotiskt tryck i omgivningen på kondrocytfunktionen
I nativt brosk skiljer sig jonkoncentrationen avsevärt från den i andra vävnader: natriumhalten i det extracellulära mediet är 250–350 mmol och dess osmolaritet är 350–450 mosmol. När kondrocyter isoleras från ECM och inkuberas i standardmedium (DMEM (Dulbeccos Minimal Essential Medium), osmolariteten är 250–280,7 mosmol) förändras miljön kring cellerna dramatiskt. Dessutom är koncentrationen av kalcium och kalium i standardmedium betydligt lägre än i nativ vävnad, och koncentrationen av anjoner är betydligt högre.
Tillsats av sackaros till mediet ökar dess osmolaritet och inducerar en övergående intracellulär ökning av koncentrationen av H + och kalciumanjoner i cytosolen. Sådana intracellulära förändringar kan påverka processerna för kondrocytdifferentiering och deras metaboliska aktivitet. J. Urban et al. (1993) fann att inkorporeringen av 358 -sulfat och 3H -prolin av isolerade kondrocyter inkuberade i standard DMEM i 2-4 timmar endast var 10% av den i nativ vävnad. Syntesintensiteten nådde ett maximum vid en osmolaritet i det extracellulära mediet på 350-400 mosmol både i nyligen isolerade kondrocyter och i broskvävnadsexplantat. Dessutom ökade volymen av kondrocyter med 30-40% efter att de isolerade cellerna placerats i standard DMEM med den specificerade osmolariteten. När kondrocyter odlas under förhållanden med icke-fysiologisk osmolaritet i 12–16 timmar anpassar sig dock cellerna till de nya förhållandena, vilket minskar biosyntesintensiteten i proportion till förändringen i osmolaritet i den extracellulära miljön.
P. Borgetti et al. (1995) studerade effekten av osmolaritet i extracellulärt medium på tillväxt, morfologi och biosyntes hos griskondrocyter. Författarna visade liknande biokemiska och morfologiska egenskaper hos kondrocyter odlade i medier med osmolaritet på 0,28 och 0,38 mosmol. Vid en medelosmolaritet på 0,48 mosmol observerades en minskning av cellproliferation och proteinsyntes under de första 4–6 timmarna av odlingen, men dessa parametrar återhämtade sig sedan och nådde så småningom kontrollvärden. När kondrocyter odlades i ett medium med en osmolaritet på 0,58 mosmol förlorade cellerna förmågan att upprätthålla den fysiologiska intensiteten hos proliferativa processer, och efter 6 dagar minskade antalet kondrocyter signifikant. Vid en medelosmolaritet på 0,58 mosmol observerades en djupgående hämning av proteinsyntesen. Dessutom, när kondrocyter odlas i medier med en osmolaritet på 0,28-0,38 mOsm, behåller de sin fysiologiska fenotyp; vid högre osmolaritet (0,48-0,58 mOsm) sker signifikanta förändringar i cellmorfologin, vilket manifesteras genom förlust av den karakteristiska fenotypen, omvandling av kondrocyter till fibroblastliknande celler och förlust av cellernas förmåga att sammansätta matrixproteoglykaner. Resultaten av denna studie indikerar kondrocyters förmåga att reagera på begränsade fluktuationer i osmolariteten i den extracellulära miljön.
Förändringar i koncentrationen av andra joner kan också påverka biosyntesprocesserna i kondrocyter. Således ökar graden av 35S (sulfat)-inkorporering med hälften med en ökning av koncentrationen av kaliumjoner från 5 mmol (koncentrationen i standard DM EM-medium) till 10 mmol (koncentrationen i ECM in vivo). Kalciumkoncentrationer under 0,5 mmol främjade kollagenproduktion av mogna bovina kondrocyter, medan en koncentration på 1-2 mmol (motsvarande koncentrationen i standard DM EM-medium) orsakade en signifikant minskning av kollagensyntesen. En måttlig ökning av biosyntesen observerades vid höga kalciumnivåer (2-10 mmol). Olika katjoner deltar i kondrocyters bindning till ECM-proteiner. Således binder magnesium- och manganjoner till fibronektin och typ II-kollagen, medan kalciumjoner inte deltar i kondrocyters bindning till proteiner. Resultaten av de beskrivna studierna indikerar således inverkan av förändringar i extracellulära joner av kalium, natrium, kalcium och osmolaritet i mediet på den biosyntetiska funktionen hos kondrocyter inkuberade i standardmedium.
Effekt av mekanisk stress på kondrocytmetabolism
Ledimmobilisering orsakar reversibel broskatrofi, vilket indikerar behovet av mekaniska stimuli för normala metaboliska processer i ledbrosk (ECM). I de flesta fall existerar de cellodlingsmodeller som används under normalt atmosfärstryck. M. Wright et al. (1996) visade att den mekaniska miljön påverkar kondrocyternas metabolism, cellresponsen beror på intensiteten och frekvensen av tryckbelastning. Experiment med belastning på explantat av intakt ledbrosk in vitro visade en minskning av syntesen av proteiner och proteoglykaner under inverkan av statisk belastning, medan dynamisk belastning stimulerar dessa processer. De exakta mekanismerna för effekten av mekanisk belastning på brosk är komplexa och är förmodligen förknippade med celldeformation, hydrostatiskt tryck, osmotiskt tryck, elektrisk potential och ytcellulära receptorer för matrixmolekyler. För att studera effekten av var och en av dessa parametrar är det nödvändigt att skapa ett system där en parameter kan varieras oberoende. Till exempel är explantatkultur inte lämplig för att studera celldeformation, men den kan användas för att studera den allmänna effekten av tryck på kondrocyternas metaboliska aktivitet. Kompression av brosk leder till celldeformation och åtföljs också av uppkomsten av en hydrostatisk tryckgradient, elektrisk potential, vätskeflöde och förändringar i sådana fysikalisk-kemiska parametrar som vattenhalten i matrisen, elektrisk laddningstäthet och osmotisk trycknivå. Celldeformation kan studeras med hjälp av isolerade kondrocyter nedsänkta i agaros- eller kollagengel.
Flera system har utvecklats för att studera effekten av mekanisk stimulering på kondrocytkultur. Vissa forskare använder system där tryck appliceras på cellkulturen genom gasfasen. Således observerade JP Veldhuijzen et al. (1979), med användning av ett tryck 13 kPa över atmosfärstryck med en låg frekvens (0,3 Hz) i 15 minuter, en ökning av syntesen av cAMP och proteoglykaner och en minskning av DNA-syntesen. R. Smith et al. (1996) visade att intermittent exponering av en kultur av primära bovina kondrocyter för hydrostatiskt tryck (10 MPa) med en frekvens på 1 Hz i 4 timmar orsakade en ökning av syntesen av aggrekan och typ II-kollagen, medan konstant tryck inte påverkade dessa processer. Med hjälp av ett liknande system rapporterade Wright et al. (1996) att cykliskt tryck på cellkultur är associerat med hyperpolarisering av kondrocytcellmembranet och aktivering av Ca2 + -beroende kaliumkanaler. Således medieras effekterna av cykliskt tryck av sträckningsaktiverade jonkanaler i kondrocytmembranet. Kondrocyternas respons på hydrostatiskt tryck beror på cellodlingsförhållandena och frekvensen av den applicerade belastningen. Således minskar cykliskt hydrostatiskt tryck (5 MPa) sulfatinkorporeringen i kondrocytmonolagern vid en frekvens av 0,05, 0,25 och 0,5 Hz, medan vid en frekvens större än 0,5 Hz ökar sulfatinkorporeringen i broskexplantatet.
M. Bushmann et al. (1992) rapporterade att kondrocyter i agarosgeler förändrar biosyntesen som svar på statisk och dynamisk mekanisk belastning på samma sätt som det odlade intakta organet. Författarna fann att mekanisk belastning genererar en hyperosmotisk stimulus med en efterföljande minskning av pH i kondrocyter.
Effekten av mekanisk sträckning kan studeras på en cellkultur nedsänkt i en gel. Sträckningskraften kan skapas med hjälp av ett datorstyrt vakuum. När systemet är under en viss grad av vakuum, förlängs botten av petriskålen med cellkulturen med en känd mängd, deformationen är maximal vid kanterna av skålens botten och minimal i mitten. Sträckningen överförs också till kondrocyterna som odlas i petriskålen. Med hjälp av denna metod visade K. Holm-vall et al. (1995) att i kondrosarkomceller odlade i en kollagen (typ II) gel ökar uttrycket av mRNA av ett 2β-integrin . Ett 2β-integrin kan binda till typ II-kollagen. Det anses vara en mekanoreceptor, eftersom det interagerar med aktinbindande proteiner och därmed förbinder ECM och cytoskelettet.
Effekten av pH på kondrocytmetabolism
PH-värdet i interstitialvätskan i ECM i broskvävnad är surare än i andra vävnader. A. Maroudas (1980) bestämde pH-värdet i ledbroskmatrixen till 6,9. B. Diamant et al. (1966) fann ett pH på 5,5 under patologiska förhållanden. Det är känt att kondrocyter lever vid låg PO2, vilket indikerar glykolysens viktiga roll (95 % av all glukosmetabolism) i dessa cellers metabolism; glykolysen åtföljs av produktionen av en stor mängd mjölksyra.
Förutom försurning av miljön genom glykolysprodukter är själva matriskomponenterna av stor betydelse. Den stora mängden fast negativ laddning på proteoglykaner modifierar den extracellulära jonsammansättningen: en hög koncentration av fria katjoner (t.ex. H +, Na +, K + ) och en låg koncentration av anjoner (t.ex. O2, HCO3) observeras. Dessutom, under inverkan av mekanisk belastning, stöts vatten ut från ECM, vilket leder till en ökning av koncentrationen av fasta negativa laddningar och attraktion av fler katjoner till matrisen. Detta åtföljs av en minskning av pH-värdet i den extracellulära miljön, vilket påverkar det intracellulära pH-värdet och därigenom modifierar kondrocyternas metabolism. R. Wilkin och A. Hall (1995) studerade effekten av pH-värdet i den extracellulära och intracellulära miljön på biosyntesen av matrisen av isolerade bovina kondrocyter. De observerade en dubbel modifiering av matrissyntesen med en minskning av pH-värdet. En liten minskning av pH (7,4
 [ 34 ], [ 35 ], [ 36 ], [ 37 ], [ 38 ], [ 39 ], [ 40 ]
[ 34 ], [ 35 ], [ 36 ], [ 37 ], [ 38 ], [ 39 ], [ 40 ]
Inverkan av odlingsmediets sammansättning på kondrocyters metabolism
Mediet för odling av kondrocyter måste motsvara de experimentella förhållandena. På senare år har kalvserum använts för att optimera odlingsförhållandena. Vid användning av serum måste dock ett antal viktiga punkter beaktas:
- utåtriktad tillväxt av celler från vävnadens periferi i organkulturer,
- variation i sammansättningen av serum från olika serier,
- närvaron av okända komponenter i dem,
- ökad risk för interferens och artefakter när man studerar olika biologiska faktorers inverkan på cellernas metaboliska aktivitet.
Ett exempel på det senare är en studie av effekten av EGF på broskkondrocyter hos råttor. EGF stimulerade inkorporeringen av 3H -tymidin och en ökning av DNA-innehållet i kulturen. Denna effekt var mer uttalad vid låga serumkoncentrationer (<1 %), men vid höga koncentrationer (>7,5 %) försvann effekten.
Det är välkänt att syntes- och nedbrytningsnivåerna i DMEM kompletterat med kalvserum är signifikant förhöjda jämfört med in vivo-förhållanden. Skillnader mellan in vivo- och in vitro-metabolism kan bero på skillnader mellan synovialvätskan och mediet i vilket cellerna odlas. Lee et al. (1997) odlade unga bovina kondrocyter i agaros med användning av ett näringsmedium innehållande DMEM kompletterat med 20 % kalvserum och en stor mängd normal allogen synovialvätska. Närvaron av synovialvätska i mediet inducerade en ökning av mängden proteoglykaner, upp till 80 % av den totala mängden synovialvätska. Dessa resultat indikerar att synovialvätska i kultur inducerar en metabolismnivå som liknar den in vivo, med en hög nivå av glykosaminoglykansyntes och en låg nivå av celldelning.
G. Verbruggen et al. (1995) visade att syntesen av 35S -arrpeKaHa av humana kondrocyter odlade i agaros i serumfritt DMEM var 20–30 % av den syntesnivå som observerades i DMEM kompletterat med 10 % kalvserum. Författarna fastställde i vilken utsträckning IGF-1, IGF-2, TGF-R eller insulin återställde aggrekanproduktionen i serumfritt medium. Författarna drog slutsatsen att 100 ng/ml insulin, IGF-1 eller IGF-2 delvis återställde aggrekansyntesen till 39–53 % av kontrollnivån. Ingen synergism eller kumulering observerades med en kombination av de listade faktorerna. Samtidigt stimulerade 10 ng/ml TGF-R i närvaro av 100 ng/ml insulin aggrekansyntesen till 90 % eller mer av referensnivån. Slutligen påverkade inte humant serumtransferrin, ensamt eller i kombination med insulin, aggrekansyntesen. När kalvserum ersattes med bovint serumalbumin minskade innehållet av aggrekanaggregat avsevärt. Anrikning av odlingsmediet med insulin, IGF eller TGF-R återställde delvis cellernas förmåga att producera aggrekanaggregat. Dessutom kan IGF-1 och insulin upprätthålla homeostas i cellkulturer. Efter 40 dagars odling i ett medium berikat med 10-20 ng/ml IGF-1 bibehölls proteoglykansyntesen på samma nivå eller till och med högre jämfört med mediet innehållande 20 % kalvserum. Kataboliska processer fortskred långsammare i mediet berikat med IGF-1 än i mediet berikat med 0,1 % albuminlösning, men något snabbare i mediet berikat med 20 % serum. I långlivade kulturer upprätthåller 20 ng/ml IGF-1 ett stabilt celltillstånd.
D. Lee et al. (1993) jämförde effekten av odlingsmediets sammansättning (DMEM, DMEM+20 % kalvserum, DMEM+20 ng/ml IGF-1) på DNA-syntes i en broskvävnadsexplantationskultur, en monolagerkultur och i agarossuspension. Vid odling i agaros i närvaro av serum observerade författarna en tendens för kondrocyter att gruppera sig i stora kluster. Celler odlade utan serum eller med IGF-1 behöll en rund form i agaros, samlade i små grupper, men bildade inte stora aggregat. I ett monolager var DNA-syntesen signifikant högre i det seruminnehållande mediet än i mediet berikat med IGF-1; DNA-syntesen i det senare var signifikant högre än i det oberikade mediet. Inga skillnader i DNA-syntes hittades när kondrocyter odlades i agarossuspension i ett oberikat medium och i ett medium med IGF-1. Samtidigt åtföljdes odling av kondrocytsuspensioner i agaros i ett serumberikat medium av ökad inkorporering av radionukleotiden 3H -tymidin jämfört med andra medier.
C-vitamin är nödvändigt för aktivering av enzymer involverade i bildandet av en stabil spiralformad struktur hos kollagenfibriller. Kondrocyter som saknar askorbinsyra syntetiserar underhydroxylerade icke-spiralformade kollagenprekursorer, vilka utsöndras långsamt. Administrering av askorbinsyra (50 μg/ml) orsakar hydroxylering av kollagen typ II och IX och deras utsöndring i normala mängder. Tillsats av C-vitamin påverkade inte nivån av proteoglykansyntes. Därför regleras kollagensekretion oberoende av proteoglykansekretion.

