Medicinsk expert av artikeln
Nya publikationer
Arteriovenös missbildning
Senast recenserade: 04.07.2025

Allt iLive-innehåll är mediekontrollerat eller faktiskt kontrollerat för att säkerställa så mycket faktuell noggrannhet som möjligt.
Vi har strikta sourcing riktlinjer och endast länk till välrenommerade media webbplatser, akademiska forskningsinstitut och, när det är möjligt, medicinsk peer granskad studier. Observera att siffrorna inom parentes ([1], [2] etc.) är klickbara länkar till dessa studier.
Om du anser att något av vårt innehåll är felaktigt, omodernt eller på annat sätt tveksamt, välj det och tryck på Ctrl + Enter.
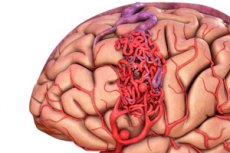
Arteriovenös missbildning är en medfödd defekt i blodkärlens utveckling, som kännetecknas av förekomsten av ett onormalt nätverk av arteriovenösa anastomoser. Oftast är arteriovenösa missbildningar belägna i den bakre kranialgropen och har en ganska typisk struktur - en eller två riktiga artärer, en härva av arteriovenösa anastomoser och en dränerande ven.
 [ 1 ]
[ 1 ]
Orsaker arteriovenös missbildning
Orsakerna som kan ligga bakom utvecklingen av AVM är inte helt klarlagda, men man tror att de kan vara relaterade till genetiska och miljömässiga faktorer. Här är några av de möjliga orsaker som kan vara förknippade med utvecklingen av AVM:
- Genetiska faktorer: Studier har visat att vissa patienter med AVM har en familjehistoria av tillståndet. Genetiska mutationer kan spela en roll i bildandet av den vaskulära abnormiteten.
- Medfödda defekter: Medfödda kärlmissbildningar kan utvecklas under embryonal utveckling. Dessa kan bero på fel i utvecklingen av hjärnans kärlvävnader.
- Miljöfaktorer: Vissa studier har visat ett samband mellan AVM och vissa miljöfaktorer, såsom strålning eller toxisk exponering under graviditet. Dessa samband är dock inte alltid bekräftade och förklarar inte alla fall av AVM.
- Regionala faktorer: I vissa fall kan AVM vara associerat med vissa geografiska områden eller etniska grupper, men dessa samband kräver ytterligare studier.
Utöver dessa faktorer som kan påverka utvecklingen av AVM är det viktigt att notera att detta är ett medfött tillstånd och vanligtvis upptäcks vid födseln eller i tidig barndom, även om symtom kan uppstå senare i livet. Ytterligare forskning behövs för att korrekt förstå orsakerna till och mekanismerna för AVM-utveckling.
Patogenes
Den farligaste är bristning av missbildningsväggarna, vilket åtföljs av spontan intrakraniell blödning. Detta sker på grund av att blandat blod cirkulerar i missbildningskärlen under tryck nära artärerna. Och naturligtvis leder högt tryck till sträckning av de degenerativt förändrade kärlen, en ökning av deras volym och en förtunning av väggen. I slutändan uppstår bristningen på det tunnaste stället. Enligt statistiska data inträffar detta hos 42-60% av patienterna med AVM. Dödligheten vid den första AVM-rupturen når 12-15%. Hos resten kan blödningen upprepas utan någon periodicitet. Vi observerade en patient som hade elva spontana intrakraniella blödningar under 8 år. Ett sådant relativt "godartat" förlopp av AVM-ruptur jämfört med bristning av arteriella aneurysmer förklaras av de särdrag som uppstår hos hemodynamiska störningar som uppstår efter rupturen. Det är känt att bristning av ett arteriellt aneurysm oftast leder till subaraknoidalblödning (SAH) och utveckling av angiospasm, som under de första minuterna är skyddande till sin natur och hjälper till att snabbt stoppa blödningen, men därefter utgör en stor fara för patientens liv.
Det är angiospasmen som leder till cerebral ischemi och ödem som avgör svårighetsgraden av patientens tillstånd och prognosen. Däremot förbättrar angiospasm i de afferenta artärerna i AVM blodtillförseln till hjärnan på grund av en minskning av arteriovenös urladdning. När en AVM brister bildas intracerebrala och subdurala hematom oftare. Blodgenombrottet in i subaraknoidalacisternerna är sekundärt. Blödningen från den rupturerade AVM-väggen stoppar snabbare, eftersom blodtrycket i den är lägre än i huvudartärerna och väggen är mer mottaglig för kompression av det spillda blodet. Naturligtvis slutar detta inte alltid bra för patienten. De farligaste AVM-rupturerna är nära hjärnans ventriklar, i de subkortikala ganglierna och i hjärnstammen. Angiospasm i de afferenta artärerna i denna situation hjälper till att stoppa blödningen.
Den avgörande faktorn i patogenesen för AVM-ruptur är volymen av spillt blod och hematomets lokalisering. Hemisfäriska intracerebrala hematom, även med en volym på upp till 60 cm3 , förlöper relativt gynnsamt. De kan orsaka allvarliga fokala neurologiska störningar, men leder sällan till allvarliga vitala störningar. Ett hematomruptur i hjärnans ventriklar försämrar prognosen avsevärt. Å ena sidan ökar blod, som irriterar ventriklarnas ependym, produktionen av cerebrospinalvätska, å andra sidan leder det till allvarliga störningar i funktionen hos vitala centra som ligger i hypotalamus. Spridningen av blod i hela ventrikulärsystemet leder till tamponad av det senare, vilket i sig är oförenligt med livet.
Blod som har trängt in i subaraknoidalacisternerna stör också cerebrospinalvätskans cirkulation, vilket gör det svårt för cerebrospinalvätskan att nå de blodblockerade pacchiongranulationerna. Som ett resultat av detta saktar ner cerebrospinalvätskans resorption och akut cerebrospinalvätskahypertension kan utvecklas, följt av intern och extern hydrocefalus. Som ett resultat av nedbrytningen av de bildade elementen från det spillda blodet bildas ett stort antal giftiga ämnen, varav de flesta har en vasoaktiv effekt. Å ena sidan leder detta till vasokonstriktion av små pialartärer, och å andra sidan ökar det kapillärpermeabiliteten. Blodnedbrytningsprodukter påverkar också nervceller, förändrar deras biokemiska processer och stör cellmembranens permeabilitet. Först och främst förändras kalium-natriumpumpens funktion och kalium börjar lämna cellen, och natriumkatjonen, som är fyra gånger mer hydrofil än kalium, rusar för att ta dess plats.
Detta leder först till intracellulärt ödem i området kring blödningen, och sedan till svullnad av cellerna. Hypoxi bidrar också till utvecklingen av ödem, vilket oundvikligen uppstår på grund av kompression av hjärnkärlen av hematomet och ökat tryck i cerebrospinalvätskan, vilket redan har nämnts. Dysfunktion i hjärnans diencefala delar och framför allt reglering av vatten-elektrolytbalansen leder till vätskeretention i kroppen, kaliumförlust, vilket också ökar hjärnans ödematösa reaktion. Patogenesen för AVM-ruptur är inte begränsad till cerebrala störningar. Inte mindre farliga är extracerebrala komplikationer. Först och främst är detta cerebrokardiellt syndrom, vilket på elektrokardiogrammet kan simulera akut koronar insufficiens.
Patienter med intracerebrala blödningar utvecklar ganska snabbt lunginflammation och andningssvikt. Dessutom spelar bakteriefloran en sekundär roll. Den primära effekten är den centrala påverkan på lungorna, bestående av utbredd bronkospasm, ökad produktion av sputum och slem, ischemi i lungparenkymet på grund av utbredd spasm i små lungartärer, vilket snabbt leder till dystrofiska störningar, deskvamation av alveolärepitelet och en minskning av lungornas gasutbytesfunktion.
Om detta åtföljs av undertryckande hostreflex, bulbär typ av andningssvikt, uppstår ett allvarligt hot mot patientens liv. I de flesta fall är den efterföljande variga trakyobronkiten dåligt mottaglig för antibakteriell behandling och förvärrar andningssvikten, vilket omedelbart påverkar en ökning av cerebral hypoxi. Således kan en kränkning av extern andning, även med relativ kompensation för cerebrala störningar, leda till döden. Ofta återfår patienter medvetandet efter koma, men dör sedan av ökande andningssvikt och hypoxiskt hjärnödem.
Dystrofiska förändringar utvecklas snabbt inte bara i lungorna, utan även i levern, mag-tarmkanalen, binjurarna och njurarna. Urinvägsinfektion och liggsår, som utvecklas snabbt i avsaknad av god patientvård, utgör ett hot mot patientens liv. Men dessa komplikationer kan undvikas om läkare kommer ihåg dem och vet hur man bekämpar dem.
Sammanfattningsvis bör undersökningen av patogenesen vid AVM-ruptur betonas att dödligheten vid sådana intrakraniella blödningar är lägre än vid ruptur av arteriella aneurysmer och hypertensiva hemorragiska stroke, även om den når 12–15 %. AVM kännetecknas av upprepade, ibland multipla blödningar med varierande periodicitet, vilket är omöjligt att förutsäga. Vid ett ogynnsamt förlopp under den posthemorragiska perioden kan de listade patogenetiska mekanismerna leda till döden.
Symtom arteriovenös missbildning
Hemorragisk typ av sjukdomen (50-70% av fallen). Denna typ kännetecknas av förekomsten av arteriell hypertoni hos patienten, en liten storlek på missbildningsnoden, dess dränering i djupa vener, arteriovenös missbildning av den bakre kranialgropen är ganska vanlig.
Hemorragisk typ är i 50 % av fallen det första symptomet på manifestation av arteriovenös missbildning, orsakar detaljerade resultat hos 10–15 % och funktionsnedsättning hos 20–30 % av patienterna (N. Martin et al.). Den årliga risken för blödning hos patienter med arteriovenös missbildning är 1,5–3 %. Risken för upprepad blödning under det första året når 8 % och ökar med åldern. Blödning från arteriovenös missbildning är orsaken till 5–12 % av all mödradödlighet och 23 % av alla intrakraniella blödningar hos gravida kvinnor. Bilden av subaraknoidalblödning observeras hos 52 % av patienterna. Hos 17 % av patienterna förekommer komplicerade former av blödning: bildandet av intracerebrala (38 %), subdurala (2 %) och blandade (13 %) hematom, hemotamponad i kamrarna utvecklas hos 47 %.
Den torpida typen av förlopp är typisk för patienter med stora arteriovenösa missbildningar lokaliserade i cortex. Blodförsörjningen till den arteriovenösa missbildningen tillhandahålls av grenar av arteria cerebri media.
De mest karakteristiska symtomen på den torpida typen av förlopp är konvulsivt syndrom (hos 26–27 % av patienterna med arteriovenös missbildning), klusterhuvudvärk och progressivt neurologiskt underskott, som vid hjärntumörer.
Varianter av kliniska manifestationer av arteriovenösa missbildningar
Som redan nämnts är den vanligaste första kliniska manifestationen av AVM spontan intrakraniell blödning (40-60% av patienterna). Det uppstår ofta utan några förstadier, mitt i fullständig hälsa. Provocerande moment kan vara fysisk ansträngning, stressande situationer, neuropsykisk spänning, intag av stora doser alkohol, etc. Vid AVM-ruptur känner patienterna en plötslig skarp huvudvärk, som ett slag eller en bristning. Smärtan ökar snabbt och orsakar yrsel, illamående och kräkningar.

Medvetslöshet kan inträffa inom några minuter. I sällsynta fall kan huvudvärken vara mild, patienterna förlorar inte medvetandet, men känner att deras lemmar försvagas och domnar (vanligtvis kontralateralt till blödningen), och talet försämras. I 15 % av fallen manifesterar sig blödningen som ett fullskaligt epileptiskt anfall, varefter patienterna kan förbli i koma.
För att bestämma svårighetsgraden av blödning från AVM kan Hunt-Hess-skalan som anges ovan användas som utgångspunkt med vissa justeringar. Eftersom blödningar från AVM kan ha mycket olika symtom, kan fokala neurologiska symtom överväga allmänna cerebrala symtom. Därför kan patienter med medvetandenivåer på I- eller II-nivåerna på skalan ha allvarliga fokala neurologiska störningar (hemipares, hemihypestesi, afasi, hemianopsi). Till skillnad från aneurysmatiska blödningar bestäms AVM-ruptur inte av svårighetsgraden och prevalensen av angiospasm, utan av volymen och lokaliseringen av det intracerebrala hematomet.
Meningealt syndrom utvecklas efter flera timmar och dess svårighetsgrad kan variera. Blodtrycket ökar vanligtvis, men inte lika kraftigt och inte lika länge som vid rupturerade arteriella aneurysmer. Vanligtvis överstiger denna ökning inte 30-40 mm Hg. På den andra eller tredje dagen uppstår hypertermi av central genes. Patienternas tillstånd försämras naturligt i takt med att hjärnödem ökar och nedbrytningen av det spillda blodet intensifieras. Detta fortsätter i upp till 4-5 dagar. Vid ett gynnsamt förlopp, efter stabilisering på den 6-8:e dagen, börjar patienternas tillstånd förbättras. Dynamiken hos fokala symtom beror på hematomets lokalisering och storlek.
Vid blödning i funktionellt viktiga områden i hjärnan eller förstörelse av motoriska ledare uppträder symtom på förlust omedelbart och kvarstår länge utan någon dynamik. Om symtomen på förlust inte uppträder omedelbart, utan ökar parallellt med hjärnödem, kan man förvänta sig att underskottet återställs inom 2-3 veckor, då ödemet helt går i regress.
Den kliniska bilden av en AVM-ruptur är ganska varierande och beror på många faktorer, varav de viktigaste är: blödningens volym och plats, svårighetsgraden av hjärnödemreaktionen och graden av involvering av hjärnstamsstrukturerna i processen.
Arteriovenösa missbildningar kan manifestera sig som epileptiforma anfall (30-40%). Orsaken till deras utveckling kan vara hemocirkulationsrubbningar i angränsande områden i hjärnan på grund av stjälfenomenet. Dessutom kan missbildningen i sig irritera hjärnbarken, vilket genererar epileptiska urladdningar. Och vi har redan pratat om vissa typer av AVM, kring vilka glios i hjärnvävnaden utvecklas, vilket också ofta manifesteras av epileptiska anfall.
Ett epileptiskt syndrom orsakat av närvaron av en AVM kännetecknas av dess orsakslösa förekomst i vuxen ålder, ofta i fullständig avsaknad av en provocerande faktor. Anfallen kan vara generaliserade eller fokala. Närvaron av en tydlig fokal komponent i ett epileptiskt anfall i avsaknad av allmänna cerebrala symtom bör väcka tanken på en möjlig AVM. Även generaliserade anfall, om de börjar med kramper huvudsakligen i samma extremiteter med en forcerad vridning av huvudet och ögonen åt ena eller andra sidan, är ofta en manifestation av en AVM. Mer sällan upplever patienter mindre anfall såsom frånvaro eller skymningsmedvetande. Frekvensen och periodiciteten hos epileptiska anfall kan variera: från isolerade till återkommande.
Formulär
VV Lebedev och medförfattare identifierade tre varianter av cerebrokardiellt syndrom baserat på EKG-data:
- Typ I - kränkning av funktionerna av automatism och excitabilitet (sinus takykardi eller bradykardi, arytmi, förmaksflimmer);
- Typ II - förändringar i repolarisationsprocesser, övergående förändringar i den slutliga fasen av det ventrikulära komplexet beroende på typen av ischemi, myokardskada med förändringar i T-vågen och ST-segmentets position;
- Typ III - ledningsfunktionsstörning (block, tecken på ökad belastning på höger hjärtmuskel). Dessa EKG-förändringar kan kombineras och deras svårighetsgrad korrelerar med svårighetsgraden av patienternas allmäntillstånd.
Komplikationer och konsekvenser
En arteriovenös missbildning (AVM) är en medfödd vaskulär anomali där artärer och vener är sammankopplade utan ett mellanliggande kapillärlager. Komplikationer och konsekvenser av AVM kan vara allvarliga och bero på storleken, platsen och egenskaperna hos den specifika missbildningen. Några av dessa inkluderar:
- Stroke: En av de allvarligaste komplikationerna vid AVM är risken för stroke. Missbildningar kan skapa onormala blodflödesvägar, vilket kan leda till blödning i hjärnan och orsaka stroke. Stroke kan ha varierande svårighetsgrad och lämna kvarvarande neurologiska brister.
- Epilepsi: AVM kan orsaka epileptiska anfall hos vissa patienter, särskilt om missbildningen är belägen i vissa områden i hjärnan.
- Blödning: Missbildningar kan vara oförutsägbara och orsaka blödning i hjärnan. Detta kan vara en livshotande komplikation och leda till allvarliga konsekvenser.
- Hydrocefalus: Om AVM är belägen nära hjärnans ventriklar kan det orsaka hydrocefalus, vilket kan leda till ansamling av extra vätska i hjärnan och ökat intrakraniellt tryck.
- Neurologiska underskott: En AVM kan skada omgivande hjärnvävnad och orsaka en mängd olika neurologiska underskott, inklusive förlamning, sensoriska störningar och underskott i tal och motorisk koordination.
- Smärta och huvudvärk: Patienter med AVM kan uppleva kronisk smärta och huvudvärk relaterad till missbildningen.
- Psykologiska effekter: Komplikationer från AVM kan ha en betydande inverkan på patienters psykologiska välbefinnande, inklusive ångest, depression och stress.
- Livsstilsbegränsningar: När en AVM upptäcks kan patienter behöva livsstilsförändringar och rekommendationer för riskhantering, inklusive att begränsa fysisk aktivitet och vissa aktiviteter.
Diagnostik arteriovenös missbildning
Diagnos av en arteriovenös missbildning (AVM) involverar vanligtvis en mängd olika bilddiagnostiska tester för att bekräfta förekomsten och utvärdera missbildningens egenskaper. De huvudsakliga metoderna som används för att diagnostisera en AVM är:
- Magnetisk resonansangiografi (MRA): MRA är en av de viktigaste metoderna för att diagnostisera AVM. Det är ett icke-invasivt test som visualiserar strukturen hos blodkärl och blodflödet i hjärnan med hjälp av magnetfält och radiovågor. MRA kan bestämma AVM:s plats, storlek och form.
- Digital subtraktionsangiografi (DSA): Detta är en mer invasiv procedur som innebär att ett kontrastmedel injiceras direkt i kärlen genom en kateter och att röntgenstrålar används för att producera högkvalitativa bilder av hjärnkärlen. DSA möjliggör en mer detaljerad undersökning av AVM-strukturen och blodflödesmönstren.
- Datortomografi (CT): CT kan användas för att upptäcka AVM och utvärdera eventuella komplikationer, såsom blödning. Vid behov kan ett kontrastmedel användas för att förbättra visualiseringen.
- Vaskulär duplexskanning (duplexultraljud): Denna teknik kan vara användbar för att undersöka kärlen i nacken och huvudet och identifiera blodflödesstörningar i samband med AVM.
- Magnetisk resonansspektroskopi (MRS): MRS kan ge information om den kemiska sammansättningen av vävnader i AVM-området och avslöja tecken på metaboliska förändringar.
- Ekoencefalografi: Detta är ett ultraljudstest som kan användas för att utvärdera blodflödet och hjärnans struktur.
- Datortomografiangiografi (CTA): CTA kombinerar datortomografi och angiografi för att producera tredimensionella bilder av blodkärlen i hjärnan.
När en AVM har diagnostiserats är det viktigt att göra en detaljerad bedömning av missbildningens egenskaper, såsom dess storlek, form och svårighetsgrad. Detta hjälper till att avgöra om behandling behövs och vilket behandlingsalternativ som är bäst, inklusive kirurgiskt avlägsnande, embolisering, strålbehandling eller observation. Beslutet att behandla en AVM bör fattas i samarbete mellan patienten och vårdteamet, med hänsyn till de individuella omständigheterna i varje enskilt fall.
Differentiell diagnos
Differentialdiagnos av arteriovenösa missbildningar (AVM) kan vara ett viktigt steg i utvärderingen av en patient med vaskulära förändringar i hjärnan. AVM är vaskulära avvikelser där artärer och vener är sammankopplade utan ett mellanliggande kapillärlager. De kan orsaka en mängd olika symtom och tillstånd, och att skilja dem från andra vaskulära sjukdomar är viktigt för korrekt behandling. Några tillstånd som kan kräva differentialdiagnos med AVM inkluderar:
- Stroke: Stroke kan efterlikna symtomen på en AVM, särskilt om stroke orsakas av vaskulära förändringar. Skillnaden kan kräva datortomografi (CT) eller magnetisk resonanstomografi (MRT) av hjärnan för att visualisera de vaskulära förändringarna.
- Hematom: Hematom, såsom subduralt eller epiduralt hematom, kan härma symtom på AVM, särskilt om de åtföljs av huvudvärk och neurologiska symtom. En datortomografi eller magnetresonanstomografi kan hjälpa till att fastställa orsaken till symtomen.
- Hjärntumörer: Hjärntumörer kan orsaka en mängd olika symtom som kan likna de vid en AVM. Diagnos kan inkludera MR med kontrastmedel och andra bildstudier.
- Migrän: Migrän med aura kan härma AVM-symtom, såsom synstörningar och yrsel. Anamnes och ytterligare tester kan hjälpa till att skilja de två åt.
- Cerebral vaskulit: Vaskulit kan orsaka inflammation i blodkärl och kärlavvikelser som kan efterlikna symtomen på en AVM. Biopsi eller angiografi kan användas för att diagnostisera vaskulit.
- Venös trombos: Venösa tromboser kan efterlikna symtomen på AVM, särskilt om det finns en störning i det venösa utflödet från hjärnan. Ytterligare studier kan hjälpa till att identifiera trombos.
För korrekt differentialdiagnos av AVM inkluderar undersökningen en omfattande klinisk undersökning, neuroedukativa metoder (CT, MRI, angiografi), ibland biopsi och andra specialiserade procedurer beroende på de specifika symtomen och omständigheterna.
Vem ska du kontakta?
Behandling arteriovenös missbildning
Behandling av en arteriovenös missbildning (AVM) beror på dess storlek, lokalisering, symtom och potentiella komplikationer. I vissa fall kan en AVM vara liten och asymptomatisk och kräver inte aktiv behandling. Men om det finns symtom eller risk för blödning kan behandling vara nödvändig. Några av behandlingarna för AVM inkluderar:
- Kirurgi: Kirurgiskt avlägsnande av AVM kan övervägas i fall där missbildningen sitter på en lättåtkomlig plats och är av låg komplexitet. Kirurgiskt avlägsnande kan bidra till att förhindra risken för blödning och minska symtom. Det är en komplex procedur och kan medföra risker såsom skador på omgivande vävnad och nerver.
Öppna (transkraniella) interventioner:
- Steg I - koagulering av afferenter;
- Steg II - isolering av kärnan i den arteriovenösa missbildningen;
- Steg III - ligering och koagulering av efferenten och avlägsnande av den arteriovenösa missbildningen,
Endovaskulära interventioner:
- stationär ballongocklusion av matningsartärer - inflödesembolisering (okontrollerad);
- kombination av tillfällig eller permanent ballongocklusion med inflödesembolisering;
- superselektiv embolisering.
Arteriovenös missbildning behandlas också med strålkirurgi (Gamma-knif, Cyber-knif, Li-nac, etc.).
- Embolisering: Embolisering är en procedur där medicinskt material eller lim förs in i blodkärl för att blockera blodflödet till den aortavertebrala ventrikulära...
- Strålbehandling: Strålbehandling kan användas för att behandla AVM, särskilt i fall där andra behandlingar kan vara för riskabla. Strålbehandling syftar till att minska blödningen i AVM och kan kräva flera sessioner.
- Medicinering: I vissa fall kan mediciner användas för att minska symtom som smärta eller kramper. Mediciner kan också användas för att kontrollera blodtrycket för att minska risken för blödning.
- Observation och symtomhantering: I vissa situationer, särskilt om AVM är liten och inte orsakar symtom, kan man besluta att helt enkelt observera tillståndet och hantera symtom efter behov.
Behandling av akuta mesotomiska sjukdomar (AVM) måste individualiseras för varje patient, och beslutet att välja en metod beror på de specifika omständigheterna. Det är viktigt att diskutera alla behandlingsalternativ med sjukvårdspersonal och göra en grundlig utvärdering av patienten för att fastställa den bästa behandlingsplanen. Behandlingsresultaten kan vara framgångsrika, och patienter kan uppnå förbättring eller fullständig återhämtning, men varje fall är unikt.
Prognos
Prognosen för en arteriovenös missbildning (AVM) beror på flera faktorer, inklusive dess storlek, lokalisering, symtom, patientens ålder och behandlingens framgång. Det är viktigt att komma ihåg att en AVM är ett medicinskt tillstånd som kan presentera sig olika hos olika patienter, och prognosen kan variera från person till person. Här är några allmänna aspekter av prognosen för en AVM:
- Risk för blödning: Den största risken med en AVM är risken för blödning (hemorragi) i hjärnan. Små AVM med låg risk för blödning kan ha en god prognos och inte orsaka allvarliga problem. Stora och medelstora AVM kan dock utgöra en betydande risk.
- Symtom: Symtom i samband med en AVM, såsom huvudvärk, kramper, förlamning eller sensoriska störningar, kan påverka prognosen. I vissa fall kan framgångsrik behandling förbättra eller eliminera symtomen.
- Storlek och placering: AVM:er som finns på farligare platser, såsom djupt inne i hjärnan eller nära kritiska strukturer, kan ha en sämre prognos. Men även många stora AVM:er kan behandlas framgångsrikt.
- Behandling: Behandling av AVM kan innefatta kirurgiskt avlägsnande, embolisering, strålbehandling eller medicinering. Framgångsrik behandling kan minska risken för blödning och förbättra prognosen.
- Ålder: Patientens ålder kan också påverka prognosen. Barn och unga vuxna har ofta en bättre prognos än äldre patienter.
- Komorbiditeter: Förekomsten av andra medicinska tillstånd eller riskfaktorer, såsom högt blodtryck eller blödningsrubbningar, kan påverka prognosen och behandlingen av AVM.
Det är viktigt att notera att AVM kräver noggrann medicinsk övervakning och behandling. Beslut om behandlingsmetod och prognos bör fattas av kvalificerade neurokirurger och neuroradiologer baserat på en omfattande utvärdering av varje enskilt fall.

