Talidomidderivat leder till att resistenta cancerceller dör
Senast recenserade: 14.06.2024

Allt iLive-innehåll är mediekontrollerat eller faktiskt kontrollerat för att säkerställa så mycket faktuell noggrannhet som möjligt.
Vi har strikta sourcing riktlinjer och endast länk till välrenommerade media webbplatser, akademiska forskningsinstitut och, när det är möjligt, medicinsk peer granskad studier. Observera att siffrorna inom parentes ([1], [2] etc.) är klickbara länkar till dessa studier.
Om du anser att något av vårt innehåll är felaktigt, omodernt eller på annat sätt tveksamt, välj det och tryck på Ctrl + Enter.
En studie utförd av Goethe-Universitetet i Frankfurt pekar på möjligheten att talidomidderivat är potentiellt lämpliga för behandling av cancer. På 1950-talet såldes talidomid som ett sömnmedel. Det blev senare ökänt för att orsaka allvarliga missbildningar hos fostret i de tidiga stadierna av graviditeten.
Molekylen är också känd för att markera proteiner i cellen för att de förstörs. Som en del av den aktuella forskningen skapade forskare derivat av talidomid. De kunde visa att dessa ämnen påverkar förstörelsen av proteiner som är ansvariga för cancercellers överlevnad.
Kanske ingen annan molekyl har ett så turbulent förflutet som talidomid. Det var huvudkomponenten i ett läkemedel som godkändes i många länder på 1950-talet som ett lugnande medel-hypnotikum. Men det stod snart klart att gravida kvinnor som tar talidomid ofta födde barn med allvarliga missbildningar.
Men under de senaste decennierna har medicinen återigen satt stora förhoppningar på det. Forskning har bland annat visat att det hämmar tillväxten av blodkärl och är därför potentiellt lämpligt för att skära bort tumörer från deras näringsmedium. Sedan visade det sig också vara mycket effektivt vid behandling av multipelt myelom, maligna tumörer i benmärgen.
"Vi vet nu att talidomid kan kallas ett 'molekylärt lim'", förklarar Dr. Xinglai Cheng från Institute of Pharmaceutical Chemistry vid Goethe-Universitetet Frankfurt. "Detta betyder att den kan ta två proteiner och sammanfoga dem."
Detta är särskilt intressant eftersom ett av dessa proteiner är en slags "märkningsmaskin": den fäster en entydig "TRASH"-etikett till ett annat protein.
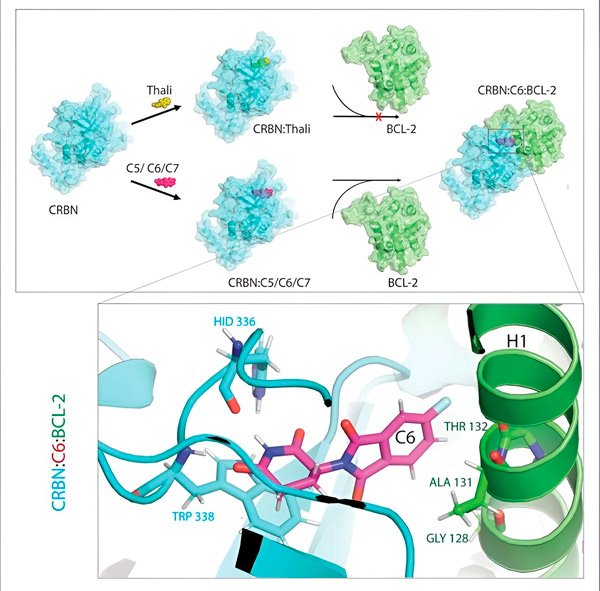
Thalidomidderivat C5, C6 och C7 modifierar CRBN, "märkningsmaskinen", så att den kan binda till BCL-2. Således är BCL-2-molekylen markerad för nedbrytning - en möjlig ny strategi för att bekämpa cancer. Författare: Dr. Xinglai Cheng
Cellens avfallshanteringssystem känner igen denna tagg: den tar tag i den märkta proteinmolekylen och river sönder den. "Det är denna mekanism som förklarar de olika effekterna av talidomid", säger Cheng. "Beroende på vilket protein som är taggat kan detta leda till missbildningar under embryonal utveckling eller till förstörelse av maligna celler."
Denna mekanism erbjuder stora medicinska löften eftersom cancerceller är beroende av vissa proteiner för att överleva. Om de systematiskt kunde målinriktas och rivas, kan sjukdomen botas. Problemet är att molekylärt lim är ganska märkligt.
En av dess bindningspartner är alltid en cellmarkeringsmaskin, eller i vetenskapligt språkbruk, ett E3-ligas som kallas CRBN. Endast ett fåtal av de många tusen proteinerna i kroppen kan vara en andra partner - vilka beror på limmet.
"Så vi skapade en serie talidomidderivat", säger Cheng. "Vi undersökte sedan om de hade vidhäftande egenskaper och i så fall vilka proteiner de var effektiva mot." För att göra detta lade forskarna till sina derivat till alla proteiner i den odlade cellinjen. De observerade sedan vilka av dessa proteiner som sedan bröts ned i närvaro av CRBN.
"I processen identifierade vi tre derivat som kunde märka ett cellulärt protein som är mycket viktigt för nedbrytning, BCL-2", förklarar Cheng. "BCL-2 hindrar cellerna från att aktivera sitt självdestruktionsprogram, så om det saknas dör cellerna."
BCL-2 har därför länge varit i fokus för cancerforskningen. Det finns till och med redan ett läkemedel mot leukemi som heter venetoclax, vilket minskar effektiviteten av BCL-2 och därmed får de muterade cellerna att självförstöras.
"Men i många cancerceller är BCL-2 själv muterad. Som ett resultat hämmar venetoclax inte längre proteinet", säger Cheng. "Vi kunde visa att våra derivat också markerar denna muterade form för nedbrytning. Dessutom simulerade våra partners vid Max Planck Institute for Biophysics interaktionen av talidomidderivat med BCL-2 på datorn. Detta visade att derivaten binder till helt andra platser än venetoclax - ett resultat som vi senare också kunde bekräfta experimentellt."
Dessutom testade forskarna sina substanser på fruktflugor med cancerceller. Överlevnaden för flugor som behandlades på detta sätt var betydligt högre. Cheng varnar dock för att bli för upphetsad eftersom dessa resultat fortfarande är grundforskning. "Även om de visar att de modifierade talidomidmolekylerna har stor terapeutisk potential, kan vi ännu inte säga om de kommer att visa sig i praktiken vid någon tidpunkt."
Studieresultaten publicerades i tidskriften Cell Reports Physical Science.
