Nya publikationer
System för läkemedelstillförsel med slutna kretsar kan förbättra tillförseln av kemoterapi
Senast recenserade: 02.07.2025

Allt iLive-innehåll är mediekontrollerat eller faktiskt kontrollerat för att säkerställa så mycket faktuell noggrannhet som möjligt.
Vi har strikta sourcing riktlinjer och endast länk till välrenommerade media webbplatser, akademiska forskningsinstitut och, när det är möjligt, medicinsk peer granskad studier. Observera att siffrorna inom parentes ([1], [2] etc.) är klickbara länkar till dessa studier.
Om du anser att något av vårt innehåll är felaktigt, omodernt eller på annat sätt tveksamt, välj det och tryck på Ctrl + Enter.
När cancerpatienter genomgår kemoterapi beräknas doserna av de flesta läkemedel baserat på patientens kroppsyta. Detta uppskattas med hjälp av en ekvation som tar hänsyn till patientens längd och vikt. Denna ekvation formulerades 1916 baserat på data från endast nio patienter.
Denna förenklade doseringsmetod tar inte hänsyn till andra faktorer och kan resultera i att en patient får för mycket eller för lite av ett läkemedel. Som ett resultat kan vissa patienter uppleva onödig toxicitet eller otillräcklig effekt av den kemoterapi de får.
För att förbättra noggrannheten i kemoterapidoseringen har MIT-ingenjörer utvecklat en alternativ metod som gör det möjligt att anpassa dosen för varje patient. Deras system mäter mängden läkemedel i patientens kropp och matar in den informationen i en styrenhet som kan justera infusionshastigheten därefter.
Denna metod skulle kunna bidra till att kompensera för skillnader i läkemedels farmakokinetik orsakad av kroppssammansättning, genetisk predisposition, kemoterapiinducerad organtoxicitet, interaktioner med andra läkemedel och mat, och cirkadiska variationer i de enzymer som är ansvariga för att bryta ner kemoterapiläkemedel, säger forskarna.
"Genom att erkänna framsteg i förståelsen av hur läkemedel metaboliseras och tillämpa tekniska verktyg för att förenkla personlig dosering, tror vi att vi kan bidra till att förändra säkerheten och effektiviteten hos många läkemedel", säger Giovanni Traverso, docent i maskinteknik vid MIT, gastroenterolog vid Brigham and Women's Hospital och huvudförfattare till studien.
Louis DeRidder, doktorand vid MIT, är huvudförfattare till artikeln som publicerats i tidskriften Med.
Kontinuerlig övervakning
I den här studien fokuserade forskarna på ett läkemedel som heter 5-fluorouracil, vilket används för att behandla kolorektal cancer och andra cancerformer. Läkemedlet administreras vanligtvis under en 46-timmarsperiod, och doseringen bestäms med hjälp av en formel baserad på patientens längd och vikt, vilket ger en uppskattning av kroppsytan.
Denna metod tar dock inte hänsyn till skillnader i kroppssammansättning som kan påverka hur läkemedlet distribueras i kroppen, eller genetiska variationer som påverkar hur det metaboliseras. Dessa skillnader kan leda till skadliga biverkningar om för mycket av läkemedlet ges. Om inte tillräckligt med läkemedel ges kanske det inte dödar tumören som förväntat.
"Människor med samma kroppsyta kan ha väldigt olika längder och vikter, olika muskelmassa eller olika gener, men så länge längden och vikten som ingår i den ekvationen ger samma kroppsyta är deras dos identisk", säger DeRidder, doktorand inom medicinsk teknik och medicinsk fysik vid Harvard-MIT-programmet i hälsovetenskap och teknologi.
En annan faktor som kan förändra mängden läkemedel i blodet vid en given tidpunkt är dygnsrytmen i ett enzym som kallas dihydropyrimidindehydrogenas (DPD), vilket bryter ner 5-fluorouracil. Uttrycket av DPD, liksom många andra enzymer i kroppen, regleras av en dygnsrytm. Nedbrytningen av 5-FU av DPD är således inte konstant, utan varierar med tiden på dygnet. Dessa dygnsrytmer kan resultera i en tiofaldig variation i mängden 5-FU i en patients blod under en infusion.
"Genom att använda kroppsytan för att beräkna kemoterapidosen vet vi att två personer kan ha väldigt olika toxicitet från 5-fluorouracil. En patient kan ha behandlingscykler med minimal toxicitet och sedan en cykel med fruktansvärd toxicitet. Något har förändrats i hur patienten metaboliserade kemoterapin från en cykel till nästa. Vår föråldrade dosmetod fångar inte upp dessa förändringar, och patienterna lider som ett resultat", säger Douglas Rubinson, klinisk onkolog vid Dana-Farber Cancer Institute och en av författaren till artikeln.
Ett sätt att försöka kompensera för variationer i farmakokinetiken för kemoterapi är en strategi som kallas terapeutisk läkemedelsövervakning, där patienten lämnar ett blodprov i slutet av en behandlingscykel. Efter att detta prov har analyserats för läkemedelskoncentrationer kan dosen justeras, vid behov, i början av nästa cykel (vanligtvis två veckor för 5-fluorouracil).
Denna metod har visat sig leda till bättre resultat för patienter, men har inte använts i stor utsträckning för kemoterapier som 5-fluorouracil.
MIT-forskarna ville utveckla en liknande typ av övervakning, men på ett automatiserat sätt som skulle göra det möjligt att anpassa läkemedelsdoseringen i realtid, vilket skulle kunna leda till bättre resultat för patienterna.
I deras slutna system kan läkemedelskoncentrationer övervakas kontinuerligt och denna information används för att automatiskt justera infusionshastigheten för kemoterapiläkemedlet för att hålla dosen inom målintervallet.
Detta slutna system gör det möjligt att anpassa läkemedelsdoseringen för att ta hänsyn till dygnsrytmen för nivåerna av läkemedelsmetaboliserande enzymer, såväl som eventuella förändringar i patientens farmakokinetik sedan den senaste behandlingen, såsom kemoterapiinducerad organtoxicitet.
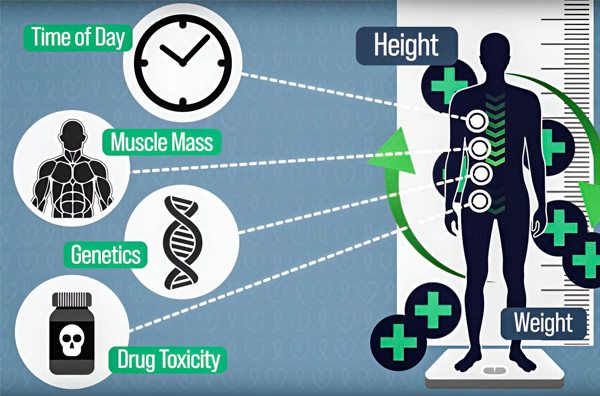
För att göra kemoterapidoseringen mer exakt har MIT-ingenjörer utvecklat ett sätt att kontinuerligt mäta mängden läkemedel i en patients kropp under en infusion som varar flera timmar. Detta kommer att bidra till att kompensera för skillnader orsakade av kroppssammansättning, genetik, läkemedelstoxicitet och cirkadiska svängningar. Källa: Med tillstånd av forskarnas tillstånd.
Det nya systemet som utvecklats av forskarna, känt som CLAUDIA (Closed-Loop AUtomated Drug Infusion regulator), använder kommersiellt tillgänglig utrustning för varje steg. Blodprover tas var femte minut och förbereds snabbt för analys. Koncentrationen av 5-fluorouracil i blodet mäts och jämförs med målintervallet.
Skillnaden mellan målkoncentrationen och den uppmätta koncentrationen matas in i en kontrollalgoritm, som sedan justerar infusionshastigheten efter behov för att bibehålla dosen inom det koncentrationsintervall där läkemedlet är effektivt och giftfritt.
"Vi har utvecklat ett system där vi kontinuerligt kan mäta läkemedelskoncentrationen och justera infusionshastigheten därefter för att bibehålla läkemedelskoncentrationen inom det terapeutiska fönstret", säger DeRidder.
Snabb justering
I djurförsök fann forskarna att de med hjälp av CLAUDIA kunde hålla mängden läkemedel som cirkulerar i kroppen inom målintervallet cirka 45 procent av tiden.
Läkemedelsnivåerna hos djur som fick kemoterapi utan CLAUDIA förblev inom målintervallet i genomsnitt endast 13 procent av fallen. Forskarna testade inte läkemedelsnivåernas effektivitet i denna studie, men att bibehålla koncentrationerna inom målfönstret tros resultera i bättre resultat och mindre toxicitet.
CLAUDIA kunde också bibehålla 5-fluorouracil-dosen inom målintervallet även när ett läkemedel som hämmar DPD-enzymet administrerades. Hos djur som fick denna hämmare utan kontinuerlig övervakning och justering ökade 5-fluorouracil-nivåerna upp till åtta gånger.
För denna demonstration utförde forskarna manuellt varje steg i processen med hjälp av standardutrustning, men planerar nu att automatisera varje steg så att övervakning och dosjusteringar kan göras utan mänsklig inblandning.
För att mäta läkemedelskoncentrationer använde forskarna högpresterande vätskekromatografi-masspektrometri (HPLC-MS), en teknik som kan anpassas för att detektera nästan alla typer av läkemedel.
"Vi ser en framtid där vi kan använda CLAUDIA för alla läkemedel som har lämpliga farmakokinetiska egenskaper och är detekterbara med HPLC-MS, vilket möjliggör personlig dosering för många olika läkemedel", säger DeRidder.
