Nya publikationer
FDA-godkända TIVDAK®: Inriktning mot vävnadsfaktor i livmoderhalscancer
Senast recenserade: 02.07.2025

Allt iLive-innehåll är mediekontrollerat eller faktiskt kontrollerat för att säkerställa så mycket faktuell noggrannhet som möjligt.
Vi har strikta sourcing riktlinjer och endast länk till välrenommerade media webbplatser, akademiska forskningsinstitut och, när det är möjligt, medicinsk peer granskad studier. Observera att siffrorna inom parentes ([1], [2] etc.) är klickbara länkar till dessa studier.
Om du anser att något av vårt innehåll är felaktigt, omodernt eller på annat sätt tveksamt, välj det och tryck på Ctrl + Enter.
Den 29 april 2024 beviljade den amerikanska läkemedelsmyndigheten (FDA) fullt godkännande för Seagen Inc.s TIVDAK® (tisotumab vedotin), ett läkemedel riktat mot vävnadsfaktor (TF), för behandling av patienter med återkommande eller metastaserande livmoderhalscancer som har progredierat under eller efter kemoterapi. Detta representerar ett betydande genombrott inom behandling av livmoderhalscancer och belyser potentialen hos antikroppsläkemedelskonjugat (ADC) inom onkologi.
Verkningsmekanism för TIVDAK
Tivdak är ett ADC som riktar sig mot TF genom att kombinera Genmabs monoklonala anti-TF-antikropp tisotumab med Seagens ADC-teknik utformad för att rikta TF-antigener på cancerceller och leverera den cytotoxiska komponenten MMAE direkt till cancerceller.
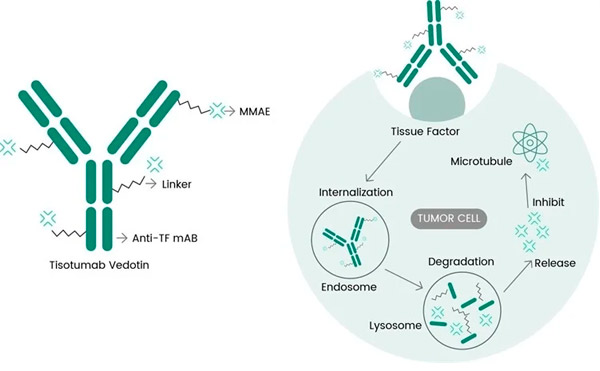
Molekylär verkningsmekanism för tisotumab vedotin ( https://doi.org/10.3390/ijms23073559 )
TF: Det perfekta målet för ADC-utveckling
TF är känt för att vara involverat i tumörsignalering och angiogenes och är överuttryckt hos den stora majoriteten av patienter med livmoderhalscancer och många andra solida tumörer. Dess förmåga att snabbt internaliseras vid antikroppsbindning och dess minimala inverkan på normal blodkoagulation ökar ytterligare dess lämplighet för riktad cancerbehandling.
