Nya publikationer
Artificiell intelligens kan utveckla behandlingar för att förhindra "superbakterier
Senast recenserade: 02.07.2025

Allt iLive-innehåll är mediekontrollerat eller faktiskt kontrollerat för att säkerställa så mycket faktuell noggrannhet som möjligt.
Vi har strikta sourcing riktlinjer och endast länk till välrenommerade media webbplatser, akademiska forskningsinstitut och, när det är möjligt, medicinsk peer granskad studier. Observera att siffrorna inom parentes ([1], [2] etc.) är klickbara länkar till dessa studier.
Om du anser att något av vårt innehåll är felaktigt, omodernt eller på annat sätt tveksamt, välj det och tryck på Ctrl + Enter.
Forskare vid Cleveland Clinic har utvecklat en modell för artificiell intelligens (AI) som kan bestämma den bästa kombinationen och tidpunkten för läkemedel för att behandla en bakteriell infektion baserat enbart på bakteriens tillväxthastighet under vissa förhållanden. Teamet, lett av Dr. Jacob Scott och hans laboratorium vid den teoretiska avdelningen för translationell hematologi och onkologi, publicerade nyligen sina resultat i tidskriften Proceedings of the National Academy of Sciences.
Antibiotika anses ha ökat den genomsnittliga livslängden i USA med nästan ett decennium. Behandlingarna minskade dödligheten i hälsoproblem som vi nu anser vara mindre, såsom vissa skärsår och skador. Men antibiotika fungerar inte längre lika bra som de en gång gjorde, delvis för att de används så flitigt.
”Globala hälsoorganisationer är överens om att vi går in i en post-antibiotikaera”, förklarar Dr Scott. ”Om vi inte förändrar hur vi bekämpar bakterier kommer fler människor att dö av antibiotikaresistenta infektioner än av cancer år 2050.”
Bakterier förökar sig snabbt och producerar muterade avkommor. Överanvändning av antibiotika ger bakterier möjlighet att utveckla mutationer som är resistenta mot behandling. Med tiden dödar antibiotika alla mottagliga bakterier och lämnar bara de starkare mutanterna kvar som antibiotika inte kan döda.
En strategi som läkare använder för att effektivisera behandlingar av bakterieinfektioner kallas antibiotikarotation. Vårdpersonal växlar mellan olika antibiotika över tid. Att växla mellan olika läkemedel ger bakterier mindre tid att utveckla resistens mot en viss antibiotikaklass. Rotation kan till och med göra bakterier mer mottagliga för andra antibiotika.
”Läkemedelsrotation visar lovande resultat för effektiv behandling av sjukdomar”, säger studiens förstaförfattare och läkarstudent Davis Weaver, PhD. ”Problemet är att vi inte vet det bästa sättet att göra det på. Det finns inga standarder för vilket antibiotikum som ska ges, hur länge eller i vilken ordning.”
Studiens medförfattare Dr. Jeff Maltas, en postdoktoral forskare vid Cleveland Clinic, använder datormodeller för att förutsäga hur bakteriers resistens mot ett antibiotikum gör dem svagare mot ett annat. Han samarbetade med Dr. Weaver för att se om datadrivna modeller kunde förutsäga läkemedelsrotationsmönster som minimerar antibiotikaresistens och maximerar känsligheten, trots den slumpmässiga naturen hos bakteriell utveckling.
Dr. Weaver ledde tillämpningen av förstärkningsinlärning på läkemedelsrotationsmodellen, som lär en dator att lära av sina misstag och framgångar för att bestämma den bästa strategin för att slutföra en uppgift. Studien är en av de första som tillämpar förstärkningsinlärning på antibiotikarotationsscheman, enligt doktorerna Weaver och Maltas.
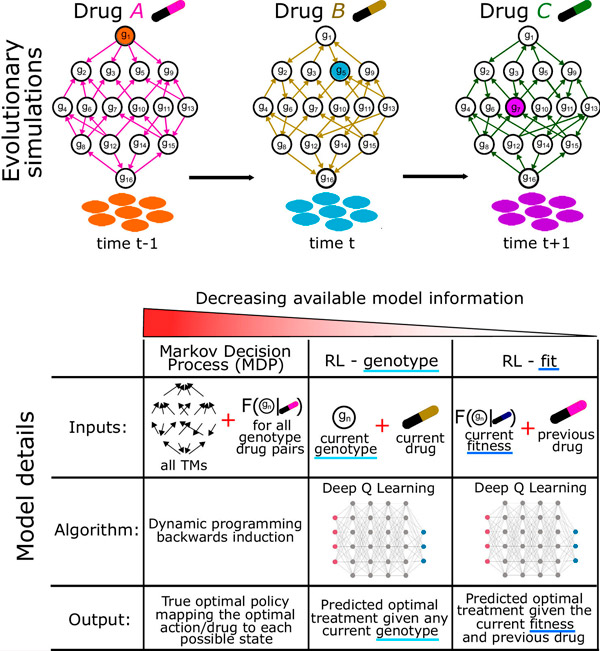
Schematisk evolutionär simulering och testade optimeringsmetoder. Källa: Proceedings of the National Academy of Sciences (2024). DOI: 10.1073/pnas.2303165121
”Förstärkande lärande är en idealisk metod eftersom man bara behöver veta hur snabbt bakterierna växer, vilket är relativt enkelt att avgöra”, förklarar Dr. Weaver. ”Det finns också utrymme för mänsklig variation och fel. Man behöver inte mäta tillväxthastigheten ner till millisekunden varje gång.”
Forskargruppens AI kunde ta fram de mest effektiva antibiotikarotationsplanerna för att behandla flera stammar av E. coli och förhindra läkemedelsresistens. Studien visar att AI kan stödja komplext beslutsfattande, såsom att beräkna antibiotikabehandlingsscheman, säger Dr. Maltas.
Dr. Weaver förklarar att utöver att hantera infektioner hos en enskild patient, skulle teamets AI-modell kunna ge information om hur sjukhus behandlar infektioner överlag. Han och hans forskargrupp arbetar också med att utöka sitt arbete bortom bakterieinfektioner till andra dödliga sjukdomar.
”Den här idén är inte begränsad till bakterier, den kan tillämpas på vilket objekt som helst som kan utveckla resistens mot behandling”, säger han. ”I framtiden tror vi att den här typen av AI skulle kunna användas för att hantera behandlingsresistenta cancerformer.”
